|
|||||||||||||||||||||||||||||||||
NỘI DUNGTác dụng, công dụng của Saponin
DƯỢC LIỆU CHỨA SAPONIN , Bồ kết Cam thảo dây Dứa Mỹ Hải sâm Khúc khắc Mạch môn Ngũ gia bě chân chim Nhân sâm Ngưu tất Rau má Tam thất Táo nhân Thięn môn Tỳ giải
|
1. Định nghĩa
Saponin
còn gọi là saponosid là một nhóm glycosid lớn, gặp rộng rãi trong
thực vật. Saponin cũng có trong một số động
vật như Hải sâm, Cá sao.
Saponin
có một số tính chất đặc biệt:
-
Làm giảm sức căng bề mặt, tạo bọt nhiều khi lắc với nước,
có tác dụng nhũ hoá và tẩy sạch.
-
Làm vỡ hồng cầu ngay ở những nồng độ rất loãng.
-
Ðộc với cá vì saponin làm tăng tính thấm của biểu mô
đường hô hấp nên làm mất các chất điện giải cần thiết,
ngoài ra có tác dụng diệt các loài thân mềm như
giun, sán,
ốc sên.
- Kích
ứng niêm mạc gây hắt hơi, đỏ mắt, có tác dụng long đờm,
lợi tiểu; liều cao gây nôn mửa, đi lỏng.
-
Có thể tạo phức với cholesterol hoặc với các chất 3-b-hydroxysteroid khác. Saponin còn gọi là saponosid do chữ latin sapo = xà phòng (vì tạo bọt như xà phòng),
Tuy
vậy một vài tính chất trên không thể hiện ở một vài
saponin.Ví dụ: sarsaparillosid thì không có tính phá huyết cũng
như tính tạo phức với cholesterol.
Saponin
đa số có vị đắng trừ một số như glycyrrhizin có trong
Cam thảo
bắc, abrusosid trong Cam thảo dây, oslandin trong cây Polypodium
vulgare có vị ngọt.
Saponin
tan trong nước, alcol, rất ít tan trong aceton, ether, hexan do đó người
ta dùng 3 dung môi này để tủa saponin. Saponin có thể bị tủa bởi
chì acetat, bari hydroxyd, ammoni sulfat.
Saponin
khó bị thẩm tích, người ta dựa vào tính chất này để tinh
chế saponin trong quá trình chiết xuất.
Phần
genin tức là sapogenin và dẫn chất acetyl sapogenin thường dễ
kết tinh hơn saponin.
Saponin
triterpenoid thì có loại trung tính và loại acid, saponin steroid thì
có loại trung tính và loại kiềm.
Về
mặt phân loại, dựa theo cấu trúc hoá học có thể chia
ra:
saponin triterpenoid và saponin steroid. 2. Cấu trúc hoá học
2.1.
Saponin triterpenoid:
Phần
genin của loại này có 30 carbon cấu tạo bởi 6 nhóm
hemiterpen.
Người ta chia làm 2 loại:
2.1.1.
Saponin triterpenoid pentacyclic: loại này chia ra các nhóm:
olean*,
ursan*, lupan*,
hopan *.
a
- Nhóm olean (I) : Phần lớn các saponin triterpenoid trong tự nhiên
đều thuộc nhóm này. Phần aglycon thường có 5 vòng và thường
là dẫn chất của 3-b hydroxy olean 12 -
ene, tức là
b-amyrin. Một vài aglycon
làm ví dụ (công thức A):
-
Acid oleanolic: R1 = R2 = R4 = R5 =
-CH3, R3 = -COOH.
-
Hederagenin: R2
= R4 = R5 = -CH3 , R1 = -CH2OH
, R3 = -COOH .
-
Gypsogenin: R2
= R4 = R5 =
-CH3 , R1 = -CHO , R3 = -COOH.
Mạch
đường có thể nối vào C-3 theo dây nối
acetal, có khi mạch
đường nối vào C-28 theo dây nối ester. Gần đây người ta
phân lập được các saponin có đến 10-11 đơn vị đường nếu
kể cả 2 mạch, riêng một mạch có thể đến 6 đơn vị đường.
b - Nhóm ursan
(II): Cấu trúc của nhóm ursan cũng tương tự
như nhóm olean chỉ khác là nhóm methyl ở C-30
không đính vào vị trí C-20 mà lại đính
ở vị trí C-19. Các sapogenin nhóm ursan thường là những dẫn
chất của 3-b hydroxy ursan 12-ene, tức là
a-amyrin. Những saponin của nhóm này ít gặp
hơn nhóm olean. Cinchona glycosid A, Cinchona glycosid B có trong cây
canh-ki-na, asiaticosid có trong rau má là những saponin của nhóm
này.
c - Nhóm lupan
(III): Cấu
trúc của nhóm lupan có các vòng A,B,C,D giống như các nhóm
trên, chỉ khác vòng E là vòng 5 cạnh, C-20 ở ngoài vòng và
thường có nối đôi ở vị trí 20-29. Lấy một ví dụ là
saponin có trong rễ cây Ô rô Acanthus iliciformis Linn.:
[a-L
- arabinofuranosyl (1-4)
b-D glucoropyranosid (1-3)]-3-b-hydroxy-lup-20(29) ene
(IIIa).
Một
số saponin có trong cây ngũ gia bì chân chim cũng thuộc nhóm này.
d - Nhóm hopan (IV):
Cấu trúc của nhóm hopan có các vòng A,B,C,D giống như các nhóm
trên, chỉ khác vòng E là vòng 5 cạnh, C-22 ở ngoài vòng và
nhóm methyl góc đính ở C-18 thay vì ở C-17. Saponin đầu tiên
được biết là chất
mollugocin A có trong cỏ thảm
Mollugo
hirta L.
2.1.2. Saponin triterpenoid
tetracyclic:
có
3 nhóm chính: dammaran*,
lanostan*,
cucurbitan.
a - Nhóm dammaran
(V): Ðại
diện là các saponin của Nhân sâm. Phần aglycon gồm 4 vòng và
một mạch nhánh. Khi tác dụng bởi acid thì mạch nhánh đóng
vòng tạo thành vòng tetrahydropyran. Bằng các phương pháp đặc
biệt để cắt phần đường, người ta đã thu được các
genin thật. Hai genin chính là:
protopanaxadiol và
protopanaxatriol.
Phần
đường nối vào OH ở cabon số 3 hoặc có khi thêm 1 mạch nữa
nối vào OH ở mạch nhánh.
Saponin triterpenoid tetracyclic nhóm damaran còn gặp trong Hạt táo (Ziziphus jujuba Mill.), Rau đắng biển (Bacopa monnieri (L.) Wettst.
b - Nhóm
lanostan (VI):
Holothurin A, một trong những saponin có trong
các loài Hải sâm - Holothuria spp. là một ví dụ của nhóm này.
Một
nhóm phụ của nhóm lanostan là nhóm cycloartan có cấu trúc 9,19
cyclo (9b)
lanostan. Các saponin abrusosid
A, B, C, D có trong cam thảo dây Abrus precatorius là những
saponin thuộc nhóm nŕy.
c/ Nhóm cucurbitan (VII). Phần lớn các saponin nhóm cucurbitan gặp trong
họ
Cucurbitaceae. Ở đây nhóm CH3 góc thay vì ở vị
trí C10 lại đính ở C9.
2.2.
Saponin steroid:
2.2.1.
Nhóm spirostan: Ta xét 3 chất sapogenin làm ví dụ:
sarsasapogenin,
smilagenin,
tigogenin. Những chất này có 27 carbon như
cholesterol, nhưng mạch nhánh từ C 20-27 tạo thành 2 vòng có oxy
(16,22 và 22,26 diepoxy), một vòng là hydrofuran (vòng E) và một
vòng là hydropyran (vòng F). Hai vòng này nối với nhau
bởi 1 carbon chung ở C-22. Mạch nhánh này được gọi là
mạch nhánh spiroacetal.
Ba
chất trên là 3 đồng phân. Smilagenin và tigogenin khác nhau do cấu
hình ở C-5. Còn sarsasapogenin và smilagenin thì khác nhau do cấu hình
ở C-25. Sarsasapogenin có nhóm methyl ở C-25 hướng axial có cấu
hình tuyệt đối 25S, smilagenin thì nhóm methyl ở C-25 hướng
equatorial có cấu hình tuyệt đối 25R.
Các
sapogenin nhóm này có nối vòng C và D trans (khác với glycosid
tim). Còn vòng A và B có thể là cis như ở chất sarsasapogenin
và smilagenin hoặc có thể là trans như ở chất
tigogenin. Công
thức lập thể của 3 chất
sarsasapogenin
Smilagenin và
tigogenin.
Nhóm
OH ở C3 thường hướng
b, một số hướng
a
ví dụ các saponin của tỳ giải.
Nhóm
spirostan hiện nay được chú ý nhiều vì là nguồn nguyên liệu
quan trọng để bán tổng hợp các thuốc steroid. Hai sapogenin quan
trọng nhất là diosgenin
(có chủ yếu trong các loài Dioscorea)
và hecogenin (có chủ yếu trong các loài
Agave).
Ở
dạng glycosid phần đường được nối vào OH ở C-3,
một số ít trường hợp ở C1. Mạch đường thường
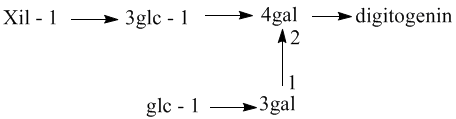
phân nhánh và phức tạp. Ví dụ digitonin là một saponosid
có trong cây digital, có mạch đường gồm 5 đơn
vị đường và phân nhánh:
2.2.2.
Nhóm furostan: Nhóm này có cấu trúc tương tự như nhóm
spirostan chỉ khác là vòng F bị biến đổi. Trường hợp thứ
nhất: vòng F mở và nhóm alcol bậc một ở C-26 được nối với
đường glucose. Nếu glucose ở C-26 bị cắt
(bởi enzym hoặc bởi
acid) thì xảy ra sự đóng vòng F thành vòng hydropyran và chuyển
thành dẫn chất nhóm spirostan. Ví dụ sarsaparillosid dưới tác
dụng của enzym thủy phân cắt mạch glucose ở C-26 sẽ chuyển
thành parillin.
Trường
hợp thứ hai: vòng F là vòng 5 cạnh do sự đóng vòng 22-25
epoxy ví dụ avenacosid có trong Yến mạch (Avena L). Họ Lúa
(Poaceae)
Avenacosid A cũng có 2 mạch đường . Khi thủy phân cắt đường
glucose ở C-26 thì cũng chuyển thành dẫn chất nhóm
spirostan.
Sarsaparillosid
và avenacosid A đều có 2 mạch đường. Người ta gọi đây là
các bidesmosid (desmos = mạch).
2.2.3. Nhóm
aminofurostan:
Ở đây vòng F mở như trường
hợp sarsaparillosid nói ở trên nhưng ở vị trí C-3 đính nhóm
NH2. Ví dụ jurubin, lŕ saponin có trong
Solanum
paniculatum
2.2.4. Nhóm
spirosolan: Nhóm này chỉ khác nhóm spirostan ở
nguyên tử oxy của vòng F được thay bằng NH. Một điểm cần
chú ý là ở đây có isomer ở C-22 (khác với nhóm
spirostan).
Ví dụ solasonin có trong cây cà Úc (= cà lá xẻ )
Solanum laciniatum có cấu trúc (25R) 22a
còn tomatin là các saponin có trong cây cà
chua thì có cấu trúc (25S) 22b.
2.2.5.
Nhóm solanidan: Solanin có trong mầm khoai tây thuộc
nhóm này. Ở đây 2 vòng E và F cùng chung 1C và 1N.
Những
chất thuộc 3 nhóm aminofurostan, spirosolan và solanidan đều có chứa
N vừa mang tính alcaloid vừa mang tính glycosid nên được gọi là
những chất glycoalcaloid. 2.2.6. Ngoài những nhóm saponin steroid kể trên người ta còn gặp một số saponin steroid có cấu trúc mạch nhánh khác ví dụ polypodosaponin và oslandin được Jizba phân lập 1971 từ thân rễ cây Polypodium vulgare L. Oslandin là một bidesmosid có vị ngọt. a-spinasterol glycosid có trong cây chè Camelia sinensis (L.) O. K.tze (Thea sinensis L.). 3. Kiểm nghiệm Saponin
CÁC PHƯƠNG PHÁP
ÐỂ KIỂM
NGHIỆM DƯỢC LIỆU CHỨA SAPONIN:
3.1.
Dựa trên tính chất tạo bọt:
Ðây là tính chất đặc trưng nhất của saponin do phân tử
saponin lớn và có cùng một lúc một đầu ưa nước và một
đầu kỵ nước. Người ta dựa trên hiện tượng gây bọt
ở môi trường kiềm và acid để sơ bộ phân biệt saponin
steroid và triterpenoid: lấy 1g bột nguyên liệu thực vật, thêm
5ml cồn, đun sôi cách thủy 15 phút.
Lấy
2 ống nghiệm cỡ bằng nhau, cho vào ống thứ nhất 5ml HCl 0,1 N
(pH=1) vào ống thứ hai 5ml NaOH 0,1 N (pH=13). Cho thêm vào mỗi ống
2-3 giọt dung dịch cồn chiết rồi bịt ống nghiệm, lắc mạnh cả
2 ống trong 15 giây. Ðể yên, nếu cột bọt trong cả 2 ống cao
ngang nhau và bền như nhau thì sơ bộ xác định trong dược liệu
có saponin triterpenoid. Nếu ống kiềm có cột bọt cao hơn ống
kia thì sơ bộ xác định là saponin steroid. Có thể dựa vào chỉ
số bọt để đánh giá một nguyên liệu chứa
saponin: chỉ số
bọt là sốml nước để hoà tan saponin trong 1g nguyên liệu cho
một cột bọt cao 1cm sau khi lắc và đọc (tiến hành trong điều
kiện qui định). Cách tiến hành: cân 1g bột nguyên liệu (qua rây
số 32), cho vào bình nón có thể tích 500ml đã chứa sẵn 100ml
nước sôi, giữ cho sôi nhẹ trong 30 phút, lọc, để nguội và
thêm nước cho đúng 100ml. Lấy 10 ống nghiệm có chiều cao 16
cm và đường kính 16 mm, cho vào các ống nghiệm lần lượt
1,2,3,...,10ml nước sắc, thêm nước cất vào mỗi ống cho đủ
mỗi ống 10ml. Bịt miệng các ống nghiệm rồi lắc theo chiều dọc
trong 15 giây, mỗi giây 2 lần lắc. Ðể yên 15 phút và đo chiều
cao của các cột bọt. Nếu cột bọt trong các ống thấp dưới
1 cm thì chỉ số bọt dưới 100. Nếu ống có cột bọt cao 1 cm nằm
giữa gam, ví dụ ống số 4 chẳng hạn thì tính như
sau: ống này
có 4ml nước sắc 1% tương ứng với 0,04g bột thì chỉ số là:
Nếu
chỉ số bọt nằm trong ống số 1, 2 thì cần pha loãng để có chỉ
số nằm giữa gam.
3.2.
Dựa trên tính chất phá huyết:
Ðây cũng là tính chất đặc trưng của
saponin. Tuy nhiên cũng
có một vài saponin không thể hiện rõ tính chất này. Khả năng
phá huyết cũng khác nhau nhiều tùy loại
saponin. Người ta cho
rằng tính phá huyết có liên quan đến sự tạo phức với
cholesterol và các ester của nó trong màng hồng cầu nhưng lại
thấy rằng giữa chỉ số phá huyết và khả năng tạo phức với
cholesterol có nhiều trường hợp không tỷ lệ thuận với nhau
nên người ta cho rằng phải xét đến ảnh hưởng của saponin
trên các thành phần khác của màng hồng cầu. Qua việc theo dõi
tính phá huyết của saponin người
ta thấy rằng cấu trúc của phần aglycon có tác dụng trực tiếp
đến tính phá huyết nhưng phần đường cũng có ảnh hưởng.
Hồng cầu của các động vật khác nhau cũng bị tác động khác
nhau đối với một saponin. Hồng cầu cừu dễ bị phá huyết nên
dùng tốt, có thể dùng máu của súc vật có sừng khác, hoặc
dùng máu thỏ thường dễ kiếm đối với các phòng thí nghiệm.
Ðể
đánh giá một nguyên liệu chứa saponin, người ta dựa trên
chỉ số phá huyết là số ml dung dịch đệm cần thiết để hoà
tan saponin có trong 1g nguyên liệu gây ra sự phá huyết đầu
tiên và hoàn toàn đối với một thứ máu đã chọn
(tiến
hành trong điều kiện qui định). Cách tiến hành:
-
Pha dung dịch đệm:
Dung dịch mono kali phosphat
9,07
% 28ml
Dung dịch dinatri phosphat 11,87 % 162ml
NaCl tinh khiết
1,8 g
-
Pha dung treo máu:
Ðể
làm cho máu không đông thì phải loại fibrin bằng cách lấy
300ml máu súc vật có sừng mới cắt tiết cho vào bình 1 lít
có miệng rộng, dùng đũa quấy tròn đều hoặc cho vào bình
một ít bi thủy tinh và lắc tròn khoảng 10 phút, lọc qua gạc
để loại fibrin, để tủ lạnh có thể dùng được vài ngày.
Từ máu đã loại fibrin này đem pha thành dung treo máu 2% với
dung dịch đệm. Có thể tiến hành chống đông máu và pha thành
dung treo máu để làm thí nghiệm bằng cách khác như
sau: Lấy
4,5ml máu thỏ trộn với 0,5ml dung dịch 3,65% Natri citrat rồi thêm
220ml dung dịch đệm.
-
Pha dung dịch saponin:
Bột
nguyên liệu đã rây qua rây 0,5 mm, cân chính xác 0,5 - 1 g, cho
vào bình, thêm dung dịch đệm (50-100ml) rồi đặt lên nồi cách
thủy (95-980C) trong 30 phút. Lọc rồi pha đến thể tích
chính xác.
-
Thử sơ bộ: Pha các hỗn hợp theo bảng dưới đây:
Lắc
nhẹ ngay hỗn hợp (tránh tạo
bọt). Sau 30 phút, lắc lại rồi để yên trong 6 giờ ở nhiệt
độ phòng. Quan sát các ống và xác định ống
(hoặc các ống)
có hiện tượng phá huyết hoàn toàn, nghĩa là ống đỏ đều
và trong, không có hồng cầu lắng đọng.
Nếu
chỉ có ống IV có hiện tượng phá huyết hoàn toàn thì cứ
dùng dung dịch dược liệu ban đầu, nếu ống III và IV có hiện
tượng phá huyết hoàn toàn thì dùng dung dịch đệm để pha
loãng gấp đôi (1:1), nếu cả 3 ống II, III, IV thì pha loãng gấp
5 (1+4), nếu cả 4 ống đều trong suốt và đỏ thì pha loãng dịch
chiết dược liệu gấp 10 lần (1+9) và làm lại thí nghiệm sơ
bộ từ đầu. Nếu trường hợp ngược lại, nghĩa là cả 4 ống
đều không có hiện tượng phá huyết hoàn toàn thì tiến hành
thử sơ bộ lại với dung dịch nguyên liệu đậm đặc hơn.
Thí nghiệm quyết định: Lấy 20 ống nghiệm nhỏ
(còn gọi là ống
phá huyết), đánh số thứ tự rồi cho vào mỗi ống lần lượt
như sau: dung dịch chiết nguyên liệu theo thứ tự tăng dần: ống
thứ nhất 0,05ml, ống thứ hai
0,10ml,..., dung dịch đệm theo thứ tư giảm dần: ống thứ nhất
0,95ml, ống thứ hai 0,90ml,..., dung treo máu 2% mỗi ống 1ml. Sau đó
lắc khẽ ngay để trộn đều. Sau 30 phút lắc lại 1 lần nữa.
Sau 24 giờ thì đọc kết quả: tìm ống đầu tiên có hiện tượng
phá huyết hoàn toàn, tính độ pha loãng của nguyên liệu trong
ống đó. Chính độ pha loãng của ống này là chỉ số phá
huyết của nguyên liệu. Có thể đọc kết quả sớm hơn bằng
cách ly tâm 10 phút (1500 vòng/phút) sau khi đã để yên 2 giờ.
3.3.
Dựa trên độ độc đối với cá:
Cá
là động vật rất nhạy cảm với saponin nên người ta dùng
các cây có saponin để thuốc cá (đừng nhầm với
rotenon). Ðể
đánh giá nguyên liệu chứa saponin, người ta có thể dựa vào
chỉ số cá. Chỉ số cá cũng phải tiến hành trong những điều
kiện quy định: môi trường, loại cá,...
D- Khả năng tạo phức với cholesterol:
Những saponin triterpenoid tạo phức kém hơn loại steroid. Trong loại
steroid thì digitonin kết hợp với cholesterol gần như hoàn toàn,
do đó digitonin được dùng làm thuốc thử để định lượng
cholesterol trong hoá sinh.
3.4.
Các phản ứng màu: Acid sulfuric đậm đặc hòa tan các saponin
và cho màu thay đổi từ vàng, đỏ, lơ-xanh lá hay lơ-tím
(phản
ứng Salkowski).
- Saponin triterpenoid cho tác dụng với vanillin 1 % trong HCl và hơ nóng
(phản ứng Rosenthaler) sẽ có màu hoa cà.
- Saponin tác dụng với antimoin trichlorid trong dung dịch chloroform rồi
soi dưới đèn phân tích tử ngoại thì saponin triterpenoid có
huỳnh quang xanh còn saponin steroid thì vàng.
Phản
ứng Liebermann-Burchardt cũng hay dùng để phân biệt 2 loại
sapogenin: lấy vài miligram sapogenin hoà nóng vào 1ml anhydrid
acetic, cho thêm 1 giọt H2SO4 đậm đặc, nếu là
dẫn chất steroid thì có màu lơ-xanh lá, còn dẫn chất
triterpenoid thì có màu hồng đến tía.
3.5.
Sắc ký lớp mỏng: Chiết xuất và tinh chế sơ bộ
saponin: đối
với saponin trung tính và acid có thể tiến hành như
sau:
bột dược liệu được chiết với ether dầu hỏa để
loại chất béo rồi chiết saponin bằng
methanol-nước (4:1). Loại
methanol dưới áp suất giảm. Hoà cặn trong nước để có dung
dịch 10% rồi lắc với n-butanol. Tách lớp n-butanol, bốc hơi
butanol dưới áp suất giảm rồi hoà cặn với methanol để có
dung dịch chấm sắc ký. Có thể tinh chế thêm bằng cách rót từ
từ dung dịch methanol vào ether có lượng lớn gấp 10-15 lần
(có
khi dùng aceton hoặc hexan thay ether).
Saponin
kiềm thuộc nhóm spirosolan và solanidan có thể chiết như
sau: bột
dược liệu thêm methanol đun nóng đến sôi trên nồi cách thủy.
Dịch lọc đem bốc hơi đến khô trên nồi cách thủy. Cắn
được hoà tan trong acid acetic 5%, đun nóng đến 800C rồi
kiềm hoá bằng ammoniac. Tủa được ly tâm rồi hoà tan vào
ethanol 96% để chấm sắc ký.
Sau
đây là một vài hệ dung môi dùng để khai triển trên các
bản mỏng silicagel-G.
Saponin
triterpenoid: a)
Chloroform-methanol-nước (65:35:10).
b) Ethyl acetat - acid acetic - nước (8:2:1).
c) n Butanol - ethanol (10:2).
Saponin
nhóm spirostan:
a) Chloroform - methanol - nước (65:35:10).
b) Chloroform - methanol (8:2).
c) n-Butanol bão hoà nước.
Saponin
kiềm: a) Chloroform - ethanol -dd.ammoniac 1%/nước (2:2:1).
b) Ethanol-pyridin-nước (3:1:3).
Cách
hiện màu: Dựa vào tính phá huyết bằng cách tráng một lớp
gelatin-máu (hoà tan 5 g gelatin trong 100ml dung dịch NaCl 9%o ở 600C, khi nguội đến 400C thì thêm máu bò đã loại fibrin)
hoặc phun dung treo máu 2% đã loại fibrin lên bản mỏng.
Các
thuốc thử dùng cho các loại saponin và sapogenin nêu dưới đây
sau khi phun cần phải sấy 10 phút ở 1100C rồi quan sát
màu ở ánh sánh thường hoặc ánh sáng tử ngoại (365nm):
thuốc thử Carr-Price (SbCl3 bão hoà trong chloroform), thuốc
thử Liebermann-Burchardt (1ml H2SO4 + 20ml anhydrid
acetic + 50ml chloroform), thuốc thử Salkowski (dung dịch acid sulfuric
10%-50% trong nước hoặc 5%-10% trong ethanol), acid phosphomolybdic 10%
trong ethanol, acid phosphotungstic 20% trong ethanol, dung dịch acid
phosphoric 50% trong nước, vanillin sulfuric (vanillin 1% trong cồn tuyệt
đối 100ml + acid sulfuric 2ml).
Saponin
nhóm spirostan còn có thể hiện màu bằng thuốc thử
Sannié (dung dịch vanillin 1% trong cồn (a), anhydrid acetic +
H2SO4
12:1 (b), phun dung dịch (a) rồi sấy 1200C trong 3 phút
sau đó phun dung dịch (b), vết saponin có màu vàng.
Ðối
với nhóm spirostan và nhóm steroid alcaloid có thể dùng thuốc
thử Carr-Price để phân biệt các dẫn chất có nối đôi và
không có nối đôi ở vị trí C-5. Các dẫn chất
D5 có màu đỏ ở 200C và tím đỏ
sau khi sấy 1050C. Cũng có thể phân biệt 2 loại dẫn
chất trên bằng thuốc thử Marquis (0,2ml dung dịch formaldehyd 37%
trong nước + 10ml H2SO4), chỉ có loại D5
cho phản ứng.
Các
saponin nhóm spirosolan và solanidan có thể phát hiện bằng thuốc
thử Dragendorff. Sắc ký đồ dịch chiết một số dược liệu chứa saponin (1) (2)
3.6.
Ðịnh lượng:
Phương pháp cân.
Chiết saponin rồi cân. Cách tiến hành chiết như trình bày ở
phần SKLM. Có khi người ta thủy phân saponin, phần sapogenin rất
ít tan trong nước được lọc hoặc được hoà tan trong dung môi
hữu cơ rồi đem bốc hơi dung môi hữu cơ, sấy, cân.
Phương
pháp đo quang. Ðối với nhóm triterpenoid có thể dùng thuốc
thử vanillin-sulfuric. Ví dụ định lượng acid glycyrrhetic trong cam
thảo, phản ứng cho màu tím.
Ðối
với nhóm spirostan, A. Akahori dùng aldehyd có nhân thơm + acid
phosphoric để định lượng: 50 mg
sapogenin + 500 mg anis aldehyd trong ethanol 99%, đun 10 phút ở
1000C để yên 1 giờ rồi đo mật độ quang ở 550 nm.
Các dẫn chất D5-sapogenin
ví dụ diosgenin thì dùng thuốc thử FeCl3-H3PO4:
800mg FeCl3 trong 10ml nước (a), lấy 1ml (a) thêm đủ 50ml
với H3PO4 (b). 50 mg diosgenin + 50ml (b) làm lạnh 5 phút
trong nước đá, thêm 0,5ml H2SO4, làm lạnh 10
phút rồi đặt trong tủ sấy ở nhiệt độ 700C trong 9
phút. Sau khi làm lạnh 10 phút và để yên 60 phút đem đo ở
485 nm. Phương pháp này có thể dùng định lượng riêng biệt
các sapogenin sau khi tách bằng sắc ký giấy hoặc sắc ký lớp
mỏng.
3.7.
Xác định bằng quang phổ: Các sapogenin triterpenoid trong
H2SO4 đậm đặc có đỉnh hấp thu cực đại trong vùng tử ngoại
ở 310 nm. Cực đại này không thể hiện với các saponin
steroid. Phổ hồng ngoại của các sapogenin steroid đặc biệt có 4 pic đặc trưng của mạch nhánh spiroacetal: pic thứ nhất ở 850 - 857 cm-1 đối với các chất 25 S hoặc 860 - 866 cm-1 đối với các chất 25 R. Pic thứ hai ở gần 900 (894-905), pic thứ ba ở gần 915 (915-923), pic thứ tư ở gần 980 (980-987). Ðể phân biệt sapogenin thuộc 25 R hoặc 25 S thì căn cứ vào cường độ hấp thu của pic thứ hai và pic thứ ba: các chất 25 R thì pic thứ hai có cường độ hấp thụ mạnh hơn pic thứ ba; đối với 25 S thì ngược lại.
4. Chiết xuất
Có
nhiều quy trình chiết xuất
khác nhau. Ta có thể tiến hành theo quy trình như đã trình bày
trong phần S.K.L.M. Ðể tinh chế, có thể thực hiện với các
phương pháp sau:
-
Thẩm tích.
-
Dùng bột Mg oxyd hoặc bột polyamid để tách saponin ra khỏi tanin:
saponin được hoà vào nước rồi trộn với bột polyamid hoặc
bột Mg oxyd trên nồi cách thủy 10 phút để có một khối nhão.
Sau đó chiết saponin từ khối nhão này bằng ethanol 80% nóng.
Lọc rồi bốc hơi.
-
Dùng Sephadex G-25,G-50,G-75: Lượng Sephadex dùng gấp 50 lần saponin
đem ngâm nước cất cho trương lên, gạn lượng nước thừa,
cho gel vào cột sắc ký.
Dung
dịch đậm đặc saponin trong nước cho lên phần trên cột rồi
khai triển bằng nước cất. Saponin có phân tử lớn sẽ ra khỏi
cột trước saponin có phân tử nhỏ.
Bằng
cách acyl hoá hoặc alkyl hoá các nhóm OH trong phân tử của các
loại Sephadex nói trên, người ta chế được các loại Sephadex
vừa có tính thân nước vừa có tính thân dung môi hữu cơ.
Ví dụ từ Sephadex G-25 bằng cách alkyl hoá người ta thu được
Sephadex LH-20 có khả năng hút được nước, alcol và cả
chloroform. Loại này dùng để tách các saponin rất hiệu quả.
-
Ðể tinh chế saponin steroid có thể dùng phương pháp kết hợp
với cholesterol: 1 g saponin hoà trong 200ml ethanol đun nóng đến
50-600C rồi cho tác dụng với một dung dịch chứa 2 g
cholesterol trong 200ml ethanol đã đun nóng, tủa phức sẽ tạo thành.
Sau khi nguội đem lọc tủa và sấy khô. Phá phức bằng cách
hoà tan trong pyridin. Saponin tinh khiết sẽ được tủa trong ether.
Ðể loại hết cholesterol, tủa được hoà tan trong methanol rồi
lại tủa với ether. - Ðể tinh chế các dẫn chất nhóm glycoalcaloid, ta hoà tan chúng vào một ít n-butanol rồi cho lên cột chứa nhôm oxyd, đẩy ra bằng nước bão hoà n-butanol. 5. Tác dụng, công dụng
-
Saponin có tác dụng long đờm, chữa ho. Saponin là hoạt chất
chính trong các dược liệu chữa ho như viễn chí, cát cánh,
cam thảo, thiên môn, mạch môn...
-
Một số dược liệu chứa saponin có tác dụng thông tiểu như
rau má, tỳ giải, thiên môn, mạch môn,...
-
Saponin có mặt trong một số vị thuốc bổ như nhân sâm, tam thất
và một số cây thuộc họ nhân sâm khác.
-
Saponin làm tăng sự thấm của tế bào; sự có mặt của
saponin sẽ làm cho các hoạt chất khác dễ hoà tan và hấp thu, ví dụ trường hợp digitonin trong
lá Digital.
-
Một số saponin có tác dụng chống viêm. Một số có tác dụng
kháng khuẩn, kháng nấm, ức chế virus.
-
Một số có tác dụng chống ung thư trên thực nghiệm.
-
Nhiều saponin có tác dụng diệt các loài thân mềm (nhuyễn thể).
-
Sapogenin steroid dùng làm nguyên liệu để bán tổng hợp các
thuốc steroid.
-
Digitonin dùng để định lượng cholesterol.
-
Một số nguyên liệu chứa saponin dùng để pha nước gội đầu,
giặt len dạ, tơ lụa.
6. Sự phân bố trong thực vật
Saponin
steroid thường gặp trong những cây một lá mầm. Các họ hay
gặp là: Amaryllidaceae, Dioscoreaceae, Liliaceae, Smilacaceae. Ðáng chú
ý nhất là một số loài thuộc chi Dioscorea
L.; Agave L.; Yucca L.
Saponin
triterpenoid thường gặp trong những cây 2 lá mầm thuộc các họ
như: Acanthaceae, Amaranthaceae, Araliaceae, Campanulaceae,
Caryophyll-aceae, Fabaceae, Polygalaceae, Rubiaceae, Sapindaceae, Sapotaceae.
Trong
cây saponin thường tích lũy ở những bộ phận khác
nhau: tích
lũy ở quả như Bồ kết, Bồ hòn; rễ như
Cam thảo, Viễn chí,
Cát cánh; lá như Dứa Mỹ... Back to Top7. Tŕi liệu tham khảoBŕi giảng Dược liệu Tập I - 1998 Dược điển Việt Nam III. Đỗ Tất Lợi - Những cây thuốc vŕ vị thuốc Việt Nam 2003 Jean BRUNETON Pharmacognosy, Phytochemistry, Medicinal Plants - Technique & Documentation - Lavoisier, 1995 (Translated by Caroline K. Hatton) Д.А. Муравьева - Фармакогнозия - Москва - Медицина 1991 Яковлев Г.П (2013) Фармакогнозия лекарственное сырье растительного и животного происхождения. 3-е изд., испр. и доп. - СПб. : СпецЛит.
Back to Top. 1. Ðịnh nghĩa, cấu trúc hoá học của Saponin 2. Các phương pháp kiểm nghiệm Dược liệu chứa Saponin 3. Phương pháp chung chiết xuất Saponin 4. Tác dụng và công dụng của Saponin 5. Các dược liệu chứa Saponin: Cam thảo, Viễn chí, Cát cánh, Ngưu tất, Nhân sâm , Tam thất 6. Diosgenin và những dược liệu dùng để chiết xuất Diosgenin. ------------------------------------------------------- Mọi thông tin lięn quan đến trang web Xin vui lňng lięn hệ theo số điện thoại 01234195602 hoặc theo địa chỉ Email: thannv@hup.edu.vn Revised: February 11, 2017 . |
||||||||||||||||||||||||||||||||