|
|
NỘI DUNGG¶m, chất nhầy vÁ cÃc polysaccarit rong biển DƯỢC LIỆU CHỨA CARBOHYDRAT Actis¶
Bạch cập
Bạch chỉ nam (Cãy)
Bạch chỉ nam (dược liệu)
Bưởi
G¶m adragant G¶m arabic Hạt Õ
Chế biến HoÁi sơn
Chế biến HoÁi sơn
Hạt tinh bột HoÁi sơn
Linh chi
Linh chi đa niõn
Linh chi đa niõn (mặt cắt)
Linh chi đa niõn (mÁu sắc)
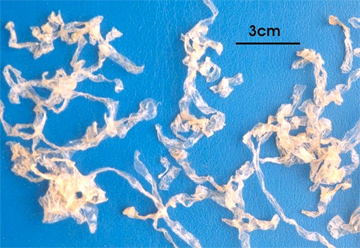
Rong sụn
Sãm bố chÚnh
Sãm bố chÚnh
Sắn
Sắn dãy
Thạch
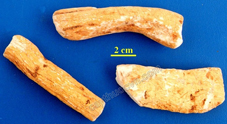
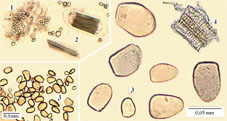
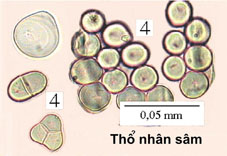
Thổ nhãn sãm
Tinh bột Thổ nhãn sãm
Tr¶m
Tinh bột biến tÚnh CMC
|
KHêI NIỆM VỀ CARBOHYDRATCarbohydrat lÁ những nhµm hợp chất hữu cơ gồm những monosaccharid, những dẫn chất vÁ những sản phẩm ngưng tụ của chºng. Carbohydrat lÁ những thÁnh phần quan trọng của thực vật. Carbohydrat lÁ nơi tÚch trữ năng lượng từ Ãnh sÃng mặt trời qua quà tršnh quang hợp, lÁ nguồn nu¶i sống loÁi người vÁ loÁi vật. (Danh phÃp quốc tế lÁ glucid, tuy nhiõn từ carbohydrat vẫn c·n được dªng tương đối phổ biến). Carbohydrat cµ thể chia thÁnh 3 nhµm: monosaccharid, oligosaccharid vÁ polysaccharid (oligo theo tiếng Hy Lạp lÁ một Út). 1. Monosaccharid lÁ những đường đơn kh¶ng thể cho carbohydrat đơn giản hơn khi bị thủy phãn, monosaccharid tồn tại trong tự nhiõn từ tetrose đến nonose. Trong thực vật chỉ một phần nhỏ monosaccarit tồn tại tự do. Phần lớn monosaccarid tồn tại ở dạng liõn kết (như trong hợp chất glucosid) 2. Oligosaccharid lÁ những carbohydrat khi thủy phãn thš cho từ 1 đến 6 đường đơn giản hơn VÚ dụ: maltose (4-O-α-D-glucopyranosyl-D-glucose), gentibiose (6-O-β-D-glucopyranosyl-D-glucose), cellobiose( 4-O-β-D-glucopyranosyl-D-glucose), lactose (4-O-β-D-glucopyranosyl-D-glucose)... 3. Polysaccharid cµ phãn tử rất lớn gồm nhiều monosaccharid nối với nhau vÚ dụ: tinh bột, cellulose, g¶m, pectin, chất nhầy... Polysaccarit lÁ cÃc carbohydrat khối lượng phãn tử cao, chºng được xem như cÃc polyme ngưng tụ trong đµ cÃc monosaccarit (hay cÃc dẫn xuất như acid uronic, đường amino) được liõn kết với nhau bằng liõn kết glucosid. Chương tršnh Dược liệu học giới thiệu chủ yếu phần polysaccharid. (Trong chương tršnh học dược liệu, để đơn giản hµa phần lớn cÃc đường đơn được dªng cÃc kỹ hiệu viết tắt: arab = arabinose, ara(f) = arabinofuranose, ara(p) = arabinopyranose; api = apiose; boi = boivinose; cym= cymarose, digin = diginose; digita = digitalose; digt = digitoxose; fuc = fucose; gal(p) = galactopyranose, gita = gitalose, glc = glucose; glcA = acid glucuronic; oleand = oleandrose; prim = primeverose; rha = rhamnose; rha(p) = rhamnopyranose; xyl = xylose. TINH BỘTTinh bột lÁ sản phẩm quang hợp của cãy xanh. Ở trong tế bÁo thực vật hạt lạp kh¶ng mÁu lÁ nơi tạo ra tinh bột, cÃc glucid h·a tan kÕo đến hạt lạp kh¶ng mÁu vÁ được để dÁnh dưới dạng tinh bột. Tinh bột được tÚch luỹ trong cÃc bộ phận của cãy như củ, rễ, quả, hạt, thãn với hÁm lượng từ 2-70%, trong là thường kh¶ng quà 1-2%. Trong quà tršnh hoạt động của cãy, tinh bột dưới tÃc động của enzym cµ sẵn trong cãy bị cắt nhỏ thÁnh những đường đơn giản ở dạng h·a tan vÁ được chuyển đến những bộ phận khÃc nhau của cãy. Trong quà tršnh di chuyển cµ thể xảy ra quà tršnh liõn kết cÃc đường tạo thÁnh tinh bột ở cÃc m¶, tổ chức của cãy. Tinh bột ở dưới dạng hạt, cµ kÚch thước vÁ hšnh dÃng khÃc nhau, kh¶ng tan trong nước lạnh, đun với nước thš tinh bột dần dần bị hồ hµa vÁ độ nhớt của dung dịch cũng tăng lõn.(Back to top) CẤU TRÖC HÆA HỌC CỦA TINH BỘT. Tinh bột được cấu tạo bởi 2 loại polysaccharid được gọi lÁ amylose vÁ amylopectin.. Amylose: phãn tử amylose lÁ một chuỗi hiện nay được biết đến hÁng ngh́šn đơn vị α-D-glucose nối với nhau theo dãy nối (1→ 4). Phãn tử amylose đa số lÁ cÃc chuỗi thẳng rất Út phãn nhÃnh. CÃc đơn vị glucose nối với nhau tạo thÁnh cÃc v·ng xoắn, mỗi v·ng cµ 6 đơn vị glucose. Amylopectin: amylopectin cµ phãn tử lượng lớn hơn khoảng 106-107 gồm 5000-50.000 đơn vị glucose vÁ phãn nhÃnh nhiều. CÃc đơn vị α-D-glucose trong mạch cũng nối với nhau theo dãy nối (1→4) c·n chỗ phãn nhÃnh thš theo dãy nối (1→6). Trong cÃc loại tinh bột, trung bšnh tỉ lệ amylose lÁ 25% c·n amylopectin lÁ 75%. Tuy nhiõn người ta cũng tạo ra được những chủng cµ nhiều amylose, vÚ dụ: Ng¶, cµ tinh bột chứa 75% amylose. Amylose cho với thuốc thử iod mÁu xanh đậm cµ cực đại phổ hấp thu khoảng 660nm, c·n amylopectin thš cµ mÁu tÚm đỏ vÁ cực đại hấp thụ khoảng 540nm. MÁu tạo thÁnh giữa tinh bột vÁ iod được giải thÚch do sự hấp phụ. Người ta cho rằng iod bị hấp phụ vÁo phÚa trong hšnh xoắn ốc. Ứng với một v·ng xoắn ốc thš cµ 1 phãn tử iod. Những phãn tử chưa đủ 6 đơn vị glucose thš kh¶ng phản ứng với iod. (Back to top) HäNH DẠNG TINH BỘT. Tinh bột tồn tại trong cãy dưới dạng hạt cµ hšnh dạng vÁ kÚch thước khÃc nhau, đãy lÁ một đặc điểm giºp Úch cho việc kiểm nghiệm một dược liệu chứa tinh bột. Tªy theo loÁi cãy vÁ tªy theo độ trưởng thÁnh của cãy mÁ hšnh dÃng vÁ kÚch thước thay đổi. Về hšnh dÃng thš cµ thể hšnh cầu, hšnh trứng, hšnh nhiều gµc ... kÚch thước cµ thể từ 1-100mm đường kÚnh. Soi kÚnh hiển vi thường thấy hạt tinh bột cấu tạo bởi nhiều lớp đồng tãm sắp xếp chung quanh một điểm gọi lÁ rốn hạt. CÃc lớp nÁy tạo nõn lÁ do hạt tinh bột lớn dần bằng cÃch tăng thõm cÃc lớp ở phÚa ngoÁi. CÃc lớp nÁy khÃc nhau ở chỉ số chiết quang vÁ hÁm lượng nước. Cµ tÃc giả cho rằng cÃc lớp khÃc nhau đµ lÁ do những lớp được tăng thõm về ban đõm vÁ những lớp tăng thõm về ban ngÁy nõn kh¶ng hoÁn toÁn giống nhau. (Bột, tinh bột) Soi kÚnh hiển vi phãn cực, hạt tinh bột cµ hšnh chữ nhật thập đen. Trong nước lạnh hšnh dạng tinh bột kh¶ng thay đổi. Khi nãng dần nhiệt độ thš tinh bột chuyển qua 3 giai đoạn. Giai đoạn đầu tinh bột ngậm một Út nước, nếu lÁm mất nước thš tinh bột trở lại t́nh trạng ban đầu. Khi nãng dần nhiệt độ khoảng 60-850C thš hạt tinh bột nở ra nhanh chµng, tinh bột ngậm nhiều phãn tử nước hơn, cÃc dãy nối hydro bị đứt. hạt tinh bột kh¶ng thể trở lại t́nh trạng ban đầu. Nếu nãng cao nhiệt độ hơn nữa thš tinh bột chuyển thÁnh hồ tinh bột. (Back to top) SỰ THỦY PHôN TINH BỘT Khi thủy phãn tinh bột bằng acid thš sản phẩm cuối cªng lÁ glucose C6H12O6 (C6H12O5)n + nH2O → (1+n) (C6H12O6) Sự thủy phãn qua cÃc chặng: dextrin, erythrodextrin, achrodextrin, maltose, glucose. Amylose dễ bị thủy phãn hơn amylopectin v́ dãy nối (1→4) dễ bị cắt hơn lÁ dãy nối (1→6). Thủy phãn bằng enzym Enzym amylase. Cµ 2 loại chÚnh: α-amylase vÁ β-amylase. Enzym α phổ biến trong cãy, nhiều nhất lÁ cÃc hạt ngũ cốc nẩy mầm, ngoÁi ra c·n cµ trong nấm mốc, nước bọt, dịch tụy. α -amylase chịu được nhiệt độ đến 700C, ở nhiệt độ nÁy thš cÃc enzym khÃc mất hoạt tÚnh. Enzym β-amylase cµ trong Khoai lang, Đậu nÁnh vÁ một số hạt ngũ cốc, chịu được nhiệt độ đến 500C nhưng chịu được m¶i trường acid cao hơn so với enzym α (pH = 3,3). Trong thực tế người ta dựa vÁo ảnh hưởng khÃc nhau đµ về độ pH vÁ nhiệt độ để tÃch 2 loại enzym trõn. Khả năng tÃc dụng lõn 2 phần của tinh bột cũng khÃc nhau: Sơ đồ phãn nhÃnh Amylopectin a) Enzym β cắt xen kẽ những dãy nối α-(1→4)-glucosid của amylose để tạo thÁnh cÃc đường maltose, kết quả thu được lÁ 100% đường maltose. Đối với amylopectin thš b-amylase chỉ cắt được cÃc dãy nối (1→4), khi gặp mạch nhÃnh thš dừng lại, kết quả tạo thÁnh maltose vÁ dextrin, lượng maltose chỉ đạt từ 50-60%. b) Enzym α cắt một cÃch ngẫu nhiõn vÁo dãy nối (1→4). Đối với amylose thš sản phẩm cuối cªng khoảng 90% lÁ maltose ngoÁi ra cµ một Út lÁ glucose. Đối với amylopectin thš a-amylase cũng chỉ tÃc động đến dãy nối (1→4) mÁ kh¶ng cắt được dãy nối (1→6) v́ thực tế người ta t́m thấy cÃc phãn tử isomaltose (= 6-O-α-D-gluco-pyranosyl-D-glucopyranose) trong dịch thủy phãn. Enzym α-amylase tiếp tục cắt được những dextrin mÁ enzym β để lại để tạo thÁnh cÃc dextrin phãn tử bÕ hơn. Như vậy a-amylase tÃc dụng lõn tinh bột thš sản phẩm thu được chủ yếu lÁ maltose rồi đến glucose vÁ dextrin phãn tử bÕ. Tinh bột nguồn gốc khÃc nhau, enzym nguồn gốc khÃc nhau thš khả năng thủy phãn cũng khÃc nhau. Khi sự thủy phãn xảy ra thš độ nhớt của dung dịch hồ tinh bột giảm dần, khả năng khử tăng lõn vÁ phản ứng với iod chuyển dần từ xanh sang tÚm rồi nãu hồng. CÃc enzym khÃc: một số enzym trong nấm mốc (Aspergillus niger, Rhizopus delemar) thủy phãn tinh bột rất tốt vÁ được sử dụng ở trong quy tršnh kỹ nghệ để chuyển tinh bột thÁnh glucose. CÃc enzym nÁy cũng tÃc động lõn dãy nối (1→4). Một số enzym nÁy lÁ: amyloglucosidase, glucoamylase, g-amylase. Enzym phosphorylase cµ trong đậu, khoai tãy, trong là vÁ cÃc bộ phận dự trữ của thực vật bậc cao. Enzym nÁy tÃc dụng lõn tinh bột để cho glucose-1-phosphat nhưng phải cµ mặt của a-amylase vÁ enzym tÃch nhÃnh như R-enzym thš sự thủy phãn mới hoÁn toÁn. Một số enzym khÃc cµ khả năng tÃc động lõn dãy nối (1→6) được gọi lÁ enzym tÃch nhÃnh vÚ dụ: R-enzym, isoamylase (cµ trong nấm men bia). (Back to top) CÃc loại hạt tinh bột hay gặp Hạt hšnh trứng vÁ hšnh thận: Tinh bột khoai tãy chế từ củ cãy khoai tãy (Solanum tuberosum L.) , thuộc họ CÁ (Solanaceae). Hạt tinh bột hšnh trứng, rốn hạt ở đầu hẹp, cÃc vãn đồng tãm dễ nhận. Thỉnh thoảng cµ hạt kÕp 2 hoặc 3. KÚch thước trung bšnh 50mm nhưng cµ hạt lớn đến 80-100mm. Tinh bột hoÁng tinh chế từ củ cãy dong riềng (Maranta arundinacea L.) , họ Dong (Marantaceae) (kh¶ng nhầm với cãy HoÁng tinh (Polygonatum sp.). Hạt hšnh trứng kÚch thước 30-60mm. Tinh bột sen, chế từ hạt cãy sen (Nelumbo nucifera Gaertn.), họ Sen (Nelumbonaceae). Hạt tinh bột hšnh trứng hay hšnh thận, rốn hạt hšnh vạch kÚch thước hạt từ 3-25mm. Tinh bột sắn (khoai mš) chế từ cãy sắn (Manihot esculenta Crantz), họ Thầu Dầu (Euphorbiaceae). Hạt hšnh cầu phần lớn một đầu bị lẹm vÁ hơi lơm tr¶ng như cÃi chu¶ng. Rốn hạt hšnh sao, kÚch thước 3-35mm. Tinh bột đậu, chế từ hạt của nhiều loại đậu (Phaseolus spp.), họ Đậu (Fabaceae). Hạt hšnh trứng hay hšnh thận. Rốn hạt dÁi vÁ phãn nhÃnh, kÚch thước trung bšnh 35mm. Tinh bột hoÁi sơn, chế từ củ của cãy Củ mÁi (Dioscorea persimilis Prain vÁ Burkill), họ Củ nãu (Dioscoreaceae). Hạt hšnh trứng hay hšnh thận. Rốn hạt dÁi, kÚch thước trung bšnh 40mm. Hạt hšnh đĩa hay hšnh thấu kÚnh dẹt: Tinh bột mš chế từ hạt của cãy lºa mš (Triticum vulgare L.), họ Lºa (Poaceae), kÚch thước hạt lớn đến 30mm, hạt bÕ 6-7mm. Tªy theo vị trÚ nhšn mÁ thấy hšnh trụ hoặc hšnh thấu kÚnh lồi 2 mặt. Rốn hạt lÁ 1 điểm ở giữa hạt, kh¶ng r¾. Hạt hšnh nhiều gµc: Tinh bột gạo chế từ hạt cãy lºa (Oriza sativa L.), họ Lºa (Poaceae). Hạt nhiều gµc, nhỏ, kÚch thước từ 4-6mm, thường được kết thÁnh đÃm. Rốn hạt kh¶ng r¾. Tinh bột ng¶ (bắp), chế từ hạt cãy ng¶ (Zea mays L.), họ Lºa (Poaceae). Hạt nhiều gµc, rốn hạt ở giữa rất r¾, kÚch thước 15-30mm. (Back to top) CHẾ TINH BỘT Phãn biệt bột với tinh bột. VÚ dụ: Bột mš, bột gạo khÃc tinh bột mš, tinh bột gạo. Muốn cµ bột mš chỉ cần nghiền nhỏ hạt lºa mš sau khi đă loại vỏ, nhưng muốn cµ tinh bột mš thš phải chế biến. ThÁnh phần của bột mš thš ngoÁi glucid c·n cµ protein, lipid, muối khoÃng, vitamin ... c·n tinh bột mš thš thÁnh phần chủ yếu lÁ glucid. Nguyõn tắc chung để chế tinh bột gồm cµ cÃc giai đoạn: 1) LÁm nhỏ nguyõn liệu để giải phµng hạt tinh bột ra khỏi cÃc tế bÁo. 2) nhÁo với nước vÁ lọc qua rãy hoặc qua vải, lấy phần dưới rãy. 3) cho lõn men. 4) rửa nước rồi phơi kh¶. Tªy loại, tÚnh chất của mỗi loai mÁ cµ phương phÃp chế biến thÚch hơp. VÚ dụ: Muốn cµ tinh bột mš thš nhÁo bột mš dưới một ḍ·ng nước, nước cuốn tinh bột đi để lại gluten lÁ một khối nhăo, dÚnh, tức lÁ phần protein. Hứng nước vÁo thªng, tinh bột lắng xuống vÁ c·n lẫn một Út gluten. Người ta cho lõn men để phãn hủy gluten bằng cÃch trộn với 1 Út nước cũ. Sau khi lõn men gạn bỏ lớp nước bõn trõn, rửa thõm 1 vÁi lần bằng nước mới rồi đem sấy hoặc phơi kh¶. Chế tinh bột gạo: Ngãm gạo hay tấm với nước v¶i trong 7 ngÁy, vớt gạo ra cho rÃo nước rồi đem xay, trong lºc xay cµ thõm nước. Nước bột xay phải đem lọc 2 lần, lần đầu qua rãy thưa, lần sau qua rãy mắt mau hơn. Tinh bột qua rãy c·n lẫn một Út protein, cần ngãm thõm với nước v¶i rồi sau đµ rửa bằng nước lă, gạn lấy tinh bột rồi phơi kh¶. (Back to top) ĐỊNH TëNH Vâ ĐỊNH LƯỢNG Để định tÚnh tinh bột chỉ cần cho tÃc dụng với dung dịch iod trong nước, tinh bột sẽ cµ mÁu xanh tÚm, cµ thể định tÚnh thẳng trõn vi phẫu để xÃc định cÃc tổ chức chứa tinh bột. Đãy lÁ phản ứng đặc trưng. Ngược lại cµ thể dªng dung dịch hồ tinh bột để phÃt hiện iod với nồng độ 2 x 10-6. Sự cµ mặt của cồn, tanin, acid nitric, chlor sẽ cản trở phản ứng. Định lượng bằng phương phÃp thủy phãn acid. Thủy phãn trực tiếp: Nguyõn liệu (2,5-3g) được rửa kỹ bằng nước cất nguội, sau đµ thủy phãn trong vÁi giờ bằng 200ml H2O vÁ 20ml HCl. LÁm nguội vÁ trung tÚnh bằng NaOH. Thõm nước đến một thể tÚch xÃc định, lấy một phần chÚnh xÃc rồi định lượng glucose tạo thÁnh vÁ suy ra lượng tinh bột. (Khối lượng glucose thu được x 0,9 = khối lượng tinh bột). Phương phÃp nÁy chỉ ứng dụng cho những nguyõn liệu chứa chủ yếu lÁ tinh bột v́ cÃc pentosan, galactan vÁ một số polysaccharid khÃc cũng bị thủy phãn cªng với tinh bột vÁ cho sai số lớn. Thủy phãn bằng enzym rồi tiếp theo bằng acid: Nguyõn tắc của phương phÃp lÁ dªng dịch chiết mạch nha (chứa cÃc enzym thủy phãn tinh bột) cho tÃc dụng lõn nguyõn liệu để chuyển tinh bột thÁnh đường h·a tan (maltose vÁ một số đường khÃc), sau đµ dªng acid để thủy phãn tiếp. Glucose tạo thÁnh sẽ được định lượng bằng một trong những phương phÃp đă được chấp nhận. Phương phÃp dựa trõn cơ sở của Purse: Phương phÃp nÁy hiện nay dªng để định lượng tinh bột trong nguyõn liệu thực vật bao gồm cÃc giai đoạn: loại đường bằng ethanol, h·a tan tinh bột bằng acid perchloric loăng vÁ nguội, tÃch tinh bột dưới dạng phức tinh bột - iod kh¶ng tan, phãn hủy phức rồi thủy phãn tinh bột thÁnh glucose vÁ định lượng glucose bằng phương phÃp tạo mÁu với anthron (mÁu xanh) hoặc bằng cÃc phương phÃp khÃc. Phương phÃp kh¶ng thủy phãn để định lượng tinh bột. Phương phÃp dªng phãn cực kế: Trong phương phÃp nÁy người ta dªng dung dịch calci chlorid đặc vÁ nµng để h·a tan tinh bột, sau đµ lÁ định lượng bằng cÃch đo độ quay cực, của dung dịch tinh bột lÁ +200. Phương phÃp tạo phức với iod: khi cho dung dịch tinh bột tÃc dụng với iod thš tạo phức cµ mÁu, cµ thể dªng để định lượng. Người ta dªng acid perchloric để h·a tan tinh bột rối cho tÃc dụng với iod, đo mÁu so sÃnh với mẫu tinh bột tinh chế. Trong phương phÃp nÁy kh¶ng cần thiết phải loại đường. Kiểm tra chất lượng Dược điển Việt Nam II tập 3 quy định kiểm tra tạp chất lạ, kim loại nặng, arsenic, giới hạn acid. CåNG DỤNG Tinh bột lÁ thÁnh phần chÚnh trong lương thực. Nguyõn liệu cµ nhiều tinh bột lÁ cÃc hạt ngũ cốc, cÃc loại củ như khoai, sắn (khoai mš), Khoai tãy Củ mÁi, Củ đao (Canna edulis Ker. Gawl.), họ Chuối hoa (Cannaceae). Cµ khi bộ phận dự trữ lại lÁ thãn cãy vÚ dụ cãy BÃng (Arenga pinnata Merr., họ Cau (Arecaceae). Hiện nay nguồn để chế tinh bột dªng trong nước vÁ xuất khẩu quan trọng nhất lÁ sắn (Manihot esculenta Crantz). Già trị xuất khẩu của 1 tấn tinh bột sắn lÁ 200 USD vÁ cứ 3,5 tấn sắn tươi thš cho 1 tấn tinh bột. Trong ngÁnh dược tinh bột được dªng lÁm tà dược viõn nÕn, dªng dạng tinh bột biến tÚnh. Tinh bột c·n lÁ nguyõn liệu để sản xuất glucose, cồn ethylic, monosodium glutamat, bÃnh kẹo... CELLULOSECellulose lÁ polysaccarid được tạo thÁnh từ cÃc đơn vị anhydroglucose lÁ thÁnh phần chÚnh của tế bÁo thực vật. Trong gỗ chứa khoảng 5% cellulose; sợi b¶ng vải 97-98%; sợi lanh, sợi gai 81-90%, sợi đay 75%, thãn cãy họ Cµi, họ Lºa 30-40%. Cellulose cũng lÁ một glucosan như tinh bột, phãn tử gồm cÃc đơn vị glucose nhưng khÃc tinh bột ở chỗ dãy nối giữa cÃc đơn vị glucose lÁ β 1→4. Khi thuỷ phãn kh¶ng hoÁn toÁn thš trong sản phẩm thuỷ phãn cµ cellotetraose, cellotriose, cellobiose vÁ khi thuỷ phãn hoÁn toÁn thš cµ glucose. Khi thuỷ phãn cellulose đă metyl hoà thš kh¶ng thu được 2,3- dimethyl glucose chứng tỏ phãn tử cellulose kh¶ng phãn nhÃnh. Khả năng khử của cellulose hết sức thấp vÁ trong sản phẩm thuỷ phãn lượng 2,3,4,6- tetramethyl glucose cũng rất Út chứng tỏ mạch của phãn tử cellulose khà dÁi. Số lượng đơn vị glucose dao động từ 3000 đến 10.000. CÃc phãn tử cellulose kết hợp nhau tạo thÁnh micel tức lÁ bµ sợi cµ chiều dÁy 50-100ż/span>. CÃc micel lại tạo thÁnh bµ microfibril với đường kÚnh khoảng 250ż/span> cµ thể thấy được bằng kÚnh hiển vi điện tử, c·n fibril tạo thÁnh từ cÃc microfibril thš cµ đường kÚnh 2000ż/span> vÁ cµ thể quan sÃt được bằng kÚnh hiển vi thường. CÃc sợi cellulose chÚnh lÁ cÃc fibril. CÃc phãn tử cellulose trong cÃc micel nhờ cµ rất nhiều liõn kết hydro nõn tạo được dạng sợi bền chắc. Cellulose kh¶ng tan trong nước vÁ dung m¶i hữu cơ nhưng tan được trong hệ dung m¶i gồm amoniac vÁ hydroxit kim loại (đãy lÁ nguyõn tắc chung để sản xuất sợi nhãn tạo). Kim loại cµ thể dªng lÁ đồng, niken, coban, cadimi... trong đµ đồng thường dªng hơn cả. Dung dịch cellulose trong phức đồng amoniac lÁm sợi rỗng chế mÁng phãn ly dªng cho thận nhãn tạo. (Back to top) CÃc dẫn chất Cellulose vÁ c¶ng dụng + Cellulose khi thuỷ phãn một phần thš thu được cellulose vi tinh thể. Đãy lÁ chất bột mÁu trắng, hạt bột cµ đường kÚnh 10-15mm, kh¶ng tan trong nước nhưng phãn tÃn được trong nước cho một gel ổn định. Bột cellulose được dªng trong bÁo chế khoa lÁm tà dược ră v́ cellulose vi tinh thể khi gặp nước nhờ cấu trºc mao quản lÁm cho nước dễ thấm vÁo viõn nÕn vÁ lÁm viõn vỡ ra. Bột cellulose c·n đµng vai tr· vừa lÁ tà dược dÚnh vừa lÁ tà dược trơn. Đãy lÁ một tà dược đa năng. Bột cellulose c·n dªng lÁm chất phãn tÃn vÁ ổn định cÃc nhũ dịch vÁ hỗn dịch. + Khi cho tÃc dụng cellulose với NaOH thš hydro của nhµm alcol bậc một của cÃc đơn vị glucose được thay thế bởi natri vÁ tạo thÁnh cellulose kiềm. Khi rửa nước thš cellulose được phục hồi nhưng cấu trºc của cÃc micel cµ thay đổi. Quà tršnh nÁy được Ãp dụng trong kỹ nghệ dệt lÁm cho sợi bµng lÃng vÁ dễ bắt mÁu khi nhuộm. + Khi cho tÃc dụng carbon disulfid (CS2) lõn cellulose thš cho cellulose xanthat . Dung dịch cao phãn tử cellulose xanthat trong nước cµ độ nhớt cao, khi bị nÕn Õp qua những lỗ nhỏ vÁo dung dịch acid sulfuric thš carbon disulfid bị loại vÁ cellulose được tÃi sinh dưới dạng sợi rất nhỏ được căng vÁ cuộn vÁo suốt chỉ. Đãy lÁ nguyõn tắc của phương phÃp sản xuất sợi cellulose tổng hợp. (Back to top) + CÃc nhµm OH của cÃc đơn vị glucose trong phãn tử cellulose cµ thể được alkyl hoÃ, vÚ dụ methyl hoà để tạo methylcellulose (MC). Việc điều chế methyl cellulose được thực hiện bằng cÃch xử l» cellulose với NaOH rồi cho methyl chlorid (CH3Cl) tÃc dụng lõn cellulose kiềm, sau đµ lÁm kết tủa methylcellulose bằng methanol, đem ly tãm rồi sấy kh¶. Tuỳ theo điều kiện phản ứng mÁ cµ tỉ lệ nhµm methoxy khÃc nhau. Methylcellulose ở dạng bột mÁu trắng, cho với nước một dung dịch giả, cµ độ nhớt thay đổi tuỳ theo nồng độ, mức độ alkyl hoÃ, độ lớn phãn tử. CÃc dung dịch giả ổn định từ pH 2 đến 12 nhưng kết tủa khi đun lõn 60oC. Trong bÁo chế người ta dªng methylcellulose trong việc bÁo chế cÃc nhũ dịch vÁ hỗn dịch, thuốc mỡ, tà dược dÚnh vÁ rÐ cho viõn nÕn. NgoÁi methylcellulose c·n cµ ethylcellulose, methy ethyl cellulose. + Hydroxy propyl methyl cellulose lÁ propylen glycol ether của methyl cellulose, trong đµ nhµm hydroxypropyl vÁ methyl đều nối vÁo cÃc đơn vị anhydroglucose của cellulose theo dãy nối ether. Trong bÁo chế khoa hydroxypropyl methyl cellulose được dªng để bÁo chế cÃc hỗn dịch. + Natri hydroxy cellulose (Na CMC) lÁ dẫn chất khÃc của cellulose. Điều chế gồm 2 giai đoạn chÚnh: cellulose được chuyển thÁnh cellulose kiềm, sau đµ cho monochloroacetat (Cl-CH2-COONa) tÃc dụng. Đãy cũng lÁ một chất bột trắng, hºt ẩm. Với nước cũng cho dung dịch giả cµ độ nhớt thay đổi tuỳ theo nồng độ, mức độ thế nhµm CH2COONa, độ lớn phãn tử . Nếu tăng pH thš độ nhớt tăng, acid hoà lÁm giảm độ nhớt vÁ tÚnh ổn định của dung dịch. Nhiệt độ tăng thš độ nhớt giảm vÁ kh¶ng kết tủa khi đun nµng trõn 60oC như MC. C¶ng dụng của NaCMC gần giống như c¶ng dụng của MC. (Back to top) + TÃc dụng cellulose với anhydrid acetic thš tạo thÁnh cellulose triacetat, tan được trong aceton vÁ cÃc ester. Cellulose acetat được sử dụng lÁm phim ảnh, nhựa dẻo, tơ acetat. + Acetophtalat cellulose lÁ ester của cellulose trong đµ cµ một số chức alcol c·n ở trạng thÃi tự do, một số khÃc bị acetyl hoà vÁ ester hoà với acid phtalic; nhµm carboxyl thứ hai của acid phtalic c·n ở dạng tự do vÁ cµ thể tạo muối. Đãy lÁ một chất bột trắng ở thể hạt, hơi cµ mªi của acid acetic, hầu như kh¶ng tan trong nước acid, tan trong m¶i trường kiềm, kh¶ng tan trong methanol vÁ chloroform, tan trong aceton, ethyl acetat vÁ trong hỗn hợp đồng thể tÚch của ethyl acetat vÁ isopropanol. (Back to top) Ưu điểm chÚnh của acetophtalat cellulose lÁ kh¶ng tan trong m¶i trường acid nõn thường được dªng để bao những thuốc kh¶ng tan trong dạ dÁy mÁ chỉ tan ở ruột. + Khi cho tÃc dụng cellulose với hỗn dịch acid nitric vÁ acid sulfuric thš tạo cellulose nitrat. Nếu nồng độ acid loăng thš ta cµ dinitrat cellulose tức lÁ colodion (hay colloxylin) tan được trong hỗn hợp cồn ether. Nếu dªng acid nitric đậm đặc vÁ acid sulfuric 95% thš ta cµ cellulose trinitrat dưới tõn lÁ pyroxylin hay b¶ng thuốc sºng (gun-cotton) lÁ nguyõn liệu của thuốc nổ. GåM, CHẤT NHẦY, PECTIN Vâ CêC POLYSACCARIT RONG BIỂNNGUỒN GỐC Vâ VAI TR̉Ø SINH Lï CỦA GåM Vâ CHẤT NHẦY. GåMG¶m tạo thÁnh trõn cãy lÁ do sự biến đổi của mÁng tế bÁo. Thường thš sự biến đổi đµ xảy ra ở những m¶ đă giÁ vÁ những m¶ đµ chuyển thÁnh g¶m, nhưng cµ khi những tế bÁo non cũng bị biến đổi. Ở những cãy thãn gỗ, g¶m tạo thÁnh do sự biến đổi những tế bÁo phần tủy hoặc tế bÁo gần vªng tầng sinh gỗ rồi chảy ra ngoÁi theo cÃc kẽ hở như lỗ sãu đục, vết chặt ... vÚ dụ trường hợp cãy mận. Ở những nơi kh¶ hanh, một số cãy tiết ra g¶m khi mªa mưa đến vÚ dụ trường hợp cãy Acacia verek mọc ở Ai Cập vªng ven sa mạc, ở đãy nửa năm kh¶ng mưa. Khi mưa xuống, cãy tiết ra g¶m ở tầng sinh gỗ. Khi kh¶ vỏ cãy nứt nẻ, g¶m theo kẽ hở tiết ra ngoÁi. е lÁ g¶m arabic. Như vậy g¶m cµ nguồn gốc bệnh l», cãy tiết ra g¶m lÁ một phản ứng đối với điều kiện kh¶ng thuận lợi. (Back to top) CHẤT NHẦYChất nhầy: KhÃi niệm "chất nhầy" dªng để chỉ cÃc phức chất polysaccarit phãn lập từ cÃc bộ phận của cãy thường tan hoÁn toÁn trong nước vÁ dung dịch kh¶ng dễ đµng rắn mặc dª độ nhớt của dung dịch cao. Một số hạt như hạt lanh, hạt một số cãy họ Hoa m¶i, khi gieo xuống đất thš sự hµa nhầy xảy ra ở toÁn bộ bõn ngoÁi của hạt lÁm cho hạt giữ nước cần thiết trong quà tršnh nảy mầm. Cµ khi chất nhầy lÁ chất dự trữ cho sự phÃt triển của bộ phận trõn mặt đất, đµ lÁ trường hợp một số cãy họ Lan - Orchidaceae mọc về mªa xuãn, vÚ dụ cãy Bạch cập. Ở cÃc loÁi tảo, chất nhầy tạo thÁnh từ những chất gian bÁo do đµ những chất nhầy gần với pectin hơn. (Back to top) Như vậy chất nhầy lÁ thÁnh phần cấu tạo của tế bÁo bšnh thường. Trong một số cãy, chất nhầy chỉ cµ mặt trong một số tế bÁo của m¶, vÚ dụ bố chÚnh sãm. Ta cũng cần biết rằng kh¶ng cµ ranh giới thật r¾ rệt giữa g¶m vÁ chất nhầy. Cµ thể quan niệm g¶m lÁ sản phẩm thu được dưới dạng rắn từ cÃc kẽ nứt tự nhiõn hay vết rạch của cãy, c·n chất nhầy lÁ sản phẩm cµ thể chiết ra từ nguyõn liệu bằng nước. Chºng ta cũng cần phãn biệt giữa g¶m vÁ chất nhựa. Về mặt hšnh dÃng bõn ngoÁi thš nhựa giống g¶m vÁ cũng chảy ra từ kẽ nứt, lỗ sãu đục hoặc vết rạch trõn cãy, vÚ dụ nhựa cÃnh kiến trắng nhưng nếu đốt chÃy, nhựa cµ mªi thơm c·n g¶m cµ mªi giấy chÃy. Nhựa kh¶ng tan trong nước nhưng dễ tan trong dung m¶i hữu cơ c·n g¶m vÁ chất nhầy khi cho vÁo trong nước sẽ nở ra vÁ tan. Về mặt hµa học, g¶m vÁ chất nhầy thuộc về polysaccharid c·n nhựa thuộc nguồn gốc terpen. Người ta cµ thể chia g¶m vÁ chất nhầy thÁnh 3 nhµm theo cấu tạo hµa học. Nhµm trung tÚnh: Nhµm nÁy về mặt cấu tạo hµa học lÁ những glactomannan hoặc glucomannan. Galactomannan lÁ cÃc polysaccharid mÁ phãn tử gồm cÃc gốc D-mannose vÁ D-galactose, glucomannan lÁ cÃc polysaccharid mÁ cÃc phãn tử gồm cÃc gốc D-mannose vÁ D-glucose. Galactomannan của mỗi loại cãy thš khÃc nhau về tỉ lệ giữa cÃc gốc galactose vÁ mannose, khÃc nhau về cấu trºc vÁ phãn tử lượng. Mạch chÚnh của cÃc phãn tử thš dÁi vÁ gồm cÃc gốc D-mannopyranose nối với nhau c·n mạch nhÃnh thš ngắn vÁ cµ cấu tạo bởi đường D-galactopyranose. VÚ dụ Guaran thš tỉ lệ giữa mannose vÁ galactose lÁ 2:1, phãn tử gồm một mạch chÚnh dÁi gồm cÃc đơn vị manose nối với nhau theo dãy nối β-(1→4) vÁ mạch nhÃnh lÁ đơn vị galactopyranose nối theo dãy nối α-(1→6) .(Back to top) Một số galactomannan khÃc thš cµ tỉ lệ giữa mannose vÁ galactose lÁ 3:1, 6:1. Loại galactomannan hay gặp ở hạt một số cãy họ Đậu, vÚ dụ galactomannan của hạt cãy cốt khÚ- Cassia occidentalis L. (đă được xÃc định cấu trºc năm 1975). Glucomannan thš hay gặp trong họ Huệ Tãy-Liliaceae, họ Lan -Orchidaceae. Về mặt cấu trºc thš loại nÁy Út được biết. Nhµm acid, thÁnh phần cµ acid uronic: Đại diện cho nhµm nÁy lÁ g¶m tiết ra ở thãn cãy, vÚ dụ g¶m arabic. Phãn tử polysaccharid của g¶m arabic cµ phãn tử lượng khoảng 250.000, phãn nhÃnh nhiều vÁ cấu tạo bởi cÃc đơn vị D-galactopyranose, L-arabinose, L-rhamnose, acid D-glucuronic theo tỉ lệ 3:3:1:1, trong đµ mạch chÚnh gồm những đơn vị D-galactopyranose nối với nhau theo dãy nối b-(1?3). Một phần lặp lại của phãn tử g¶m arabic R=L-Araf-(1?, L-Rhap- (1?, a-D-Galp-(1?3)-L-Araf-(1?, hoặc Út gặp hơn: b-L-Araf-(1?3) L-Araf-(1?. G¶m tiết ra ở thãn cãy mơ-Prunus armeniaca L. thÁnh phần gồm cµ D-xylose, L-arabinose, D-galactose theo tỉ lệ 1:8:8 ngoÁi ra c·n cµ một lượng nhỏ D-mannose vÁ acid D-glucuronic. Khi đun nµng với nước, g¶m bị thủy phãn giải phµng L-arabinose vÁ tạo thÁnh những mảnh cµ khối lượng phãn tử bÕ. Phãn tÚch cấu trºc bằng phương phÃp cắt nhỏ phãn tử vÁ bằng phương phÃp oxy hµa với periodat cho thấy phãn tử g¶m cµ một mạch chÚnh gồm cÃc đơn vị b-D-galactopyranose nối theo dãy nối (1?6), mạch chÚnh nÁy mang nhiều mạch nhÃnh ở C-3 gồm cµ cÃc đơn vị L-arabinofuranose, D-galactose vÁ acid D-glucuronic. Người ta c·n thấy rằng mạch chÚnh thỉnh thoảng cµ cÃc đơn vị L-arabinose xen vÁo. (Back to top) G¶m tiết ra ở thãn cãy ở một số loÁi thuộc chi Citrus thÁnh phần gồm cµ L-arabinose, D-galactose vÁ acid D-glucuronic. Tỉ lệ giữa cÃc đơn vị đường nÁy thay đổi tªy theo loÁi vÚ dụ g¶m của cãy chanh cµ tỉ lệ 2:5:2. AGAAlgae Gel Mask - Mặt nạ tảo biển dạng gelAlginatAlgin hay acid alginic lÁ một acid hữu cơ cµ trong tảo nãu cµ trọng lượng phãn tử từ 32.000 đến 200.000 do acid manuronic vÁ acid vÁ axit L-guluronic liõn kết với nhau bằng liõn kết 1-4 glucozit. Tỷ lệ cÃc acid nÁy trong mạch phụ thuộc vÁo loÁi, vị trÚ thu hÃi vÁ từng bộ phận trong tảo. Tỷ lệ M?G của cÃc loÁi tảo nãu lÁ 1:0,5 đến 1:3. Ở một số tảo nãu cũng cµ polysaccharid thuộc nhµm acid: acid alginic. Acid alginic cấu tạo bởi cÃc đơn vị acid guluronic vÁ acid mannuronic. Dãy nối giữa cÃc acid lÁ b-(1?4), phãn tử lượng trung bšnh khoảng 200.000. Tỉ lệ giữa cÃc acid uronic thay đổi tªy theo nguồn gốc. Tỉ lệ giữa acid mannuronic/guluronic lÁ 1,56 ở tảo Macrocystis pyrifera, 1,85 ở Ascophyllum nodosum, 0,45 ở Laminaria hyperborea. Chuỗi phãn tử polysaccharid kh¶ng đồng nhất. Qua sự thủy phãn từng phần, người ta xÃc định cµ 3 kiểu sắp xếp trong phãn tử, cµ đoạn lÁ polymannuronic, hoặc polyguluronic hoặc xen kẽ giữa 2 acid. Ở trong tảo cÃc acid ở dạng muối hỗn hợp (Na, Mg, K, Ca). (Back to top) Acid mannuronic Acid guluronic HÁng năm thế giới sản xuất đến 10.000 tấn acid alginic Nhµm acid, cµ thÁnh phần gốc sulfat. Đại diện cho nhµm nÁy lÁ thạch- Agar Agar. Thạch lÁ sản phẩm chế từ một số loÁi tảo biển. ThÁnh phần của thạch chứa chừng 70-80% polysaccharid, 10-20%nước, 1,5-4% chất v¶ cơ. Phần polysaccharid cấu tạo bởi cÃc gốc D- vÁ L- galactose, 3, 6-anhydrogalactose, cÃc pentose, acid glucuronic vÁ cÃc gốc sulfat. Người ta chia ra 2 loại polysaccharid khÃc nhau: agarose vÁ agaropectin. Agarose lÁ polysaccharid cấu tạo bởi cÃc gốc βb-D-galactopyranose theo dãy nối (1-3) luãn phiõn với 3, 6 -anhydro a-L-galactopyranose theo dãy nối (1-4) (đường đ¶i nÁy cµ tõn lÁ agarobiose) ngoÁi ra c·n cµ mặt cÃc đon vị D-galactose mang nhµm 6-O-methyl vÁ một lượng rất Út D-xylose. Agarose chiếm khoảng 55-66% vÁ cµ thể tÃch bằng cÃch kết tủa với polyethylen glycol. Agaropectin thš chiếm khoảng 40% của toÁn bộ polysaccharid, cµ cấu trºc phức tạp. ThÁnh phần cµ acid glucuronic, D-galactose, 3,4-anhydro L-galactose. Một phần của cÃc đơn vị đường được ester hµa với acid sulfuric. TëNH CHẤT G¶m vÁ chất nhầy h·a tan trong nước tạo thÁnh dung dịch keo cµ độ nhớt cao, hoÁn toÁn kh¶ng tan trong cÃc dung m¶i hữu cơ như ether, benzen, chloroform. Độ tan trong cồn thay đổi tªy theo độ cồn vÁ tuỳ theo loại g¶m hay chất nhầy, cồn cao độ thš kh¶ng tan. G¶m vÁ chất nhầy bị tủa bởi ch́ acetat trung tÚnh hoặc kiềm vÁ khÃc pectin ở chỗ kh¶ng bị tÃc động enzym pectinesterase. G¶m vÁ chất nhầy cµ tÚnh quang hoạt. Loại g¶m vÁ chất nhầy nÁo cµ cấu tạo chuỗi thẳng thš tạo được mÁng nhưng Út cµ tÚnh dÚnh, trÃi lại loại nÁo cµ cấu tạo phãn nhÃnh thš khµ tạo mÁng nhưng cµ tÚnh dÚnh cao. Độ nhớt của dung dịch thuộc nhµm trung tÚnh thš thay đổi Út theo pH c·n nhµm acid thš thay đổi theo pH. Chất nhầy bắt mÁu xanh với methylen nõn cµ thể lợi dụng để định tÚnh chất nhầy trõn vi phẫu thực vật. (Back to top) ĐêNH GIê MỘT DƯỢC LIỆU CHỨA GåM HOẶC CHẤT NHẦY. Để đÃnh già một dược liệu chứa g¶m hay chất nhầy ta cµ thể dựa vÁo phương phÃp tủa bằng cồn rồi lọc, sấy, cãn. Cµ thể tủa bằng ch́ acetat. Người ta c·n đÃnh già bằng phương phÃp đo độ nhớt. Một số dược điển quy định việc đÃnh già một số dược liệu chứa chất nhầy dựa trõn chỉ số nở: chỉ số nở lÁ thể tÚch tÚnh bằng ml mÁ 1gam dược liệu khi nở trong nước chiếm được. ThÚ nghiệm tiến hÁnh trong những điều kiện quy định: kÚch thước ống đong, lượng dược liệu, độ nhỏ của dược liệu, thời gian ngãm, nhiệt độ ... Dược điển PhÃp (năm 1972) quy định phương phÃp đÃnh già một dược liệu chứa chất nhầy như sau: tiến hÁnh trong một ống đong cµ 20cm chiều cao vÁ 2 cm đường kÚnh, chia thể tÚch bắt đầu từ đÃy. Cho 1 gam dược liệu để nguyõn hay nghiền nhỏ vÁo ống, thõm 25 ml nước, đậy nºt. Lắc nhẹ đều lºc đầu, sau đµ thỉnh thoảng lắc trong v·ng 1 giờ. Để yõn 6 giờ ở nhiệt độ 15-200C . Thể tÚch theo ml mÁ dược liệu bao gồm cả chất nhầy chiếm được chÚnh lÁ chỉ số nở. Để tÃch g¶m hoặc chất nhầy trong dược liệu, cµ thể dựa vÁo độ h·a tan trong nước rồi thõm cồn cao độ để tủa, tÃch riõng rồi tinh chế bằng phương phÃp thẩm tÚch. Muốn biết thÁnh phần monosaccharid trong cấu trºc của g¶m hay chất nhầy, ta cµ thể tiến hÁnh thủy phãn rồi xÃc định cÃc monosaccharid bằng phương phÃp sắc k». Muốn thủy phãn người ta đun g¶m hoặc chất nhầy với acid sunfuric 2N. Dung dịch đă thủy phãn sau khi trung h·a bằng bari hydroxyd dªng để phãn tÚch sắc k». (Back to top) ỨNG DỤNG. G¶m vÁ chất nhầy được ứng dụng trong kỹ nghệ dệt, thực phẩm ... Trong bÁo chế khoa g¶m thường được dªng lÁm chất nhũ hµa, lÁm tà dược. một số dược liệu chứa chất nhầy thường cµ tÃc dụng chữa ho vÁ lÁm chµng lÁnh cÃc vết thương, vết loÕt. Thạch (Agar-Agar) dªng để chữa tÃo bµn vÁ để chế m¶i trường nu¶i cấy trong khoa vi sinh. Alginat cµ tÚnh chất trương nở, kh¶ng hấp thu ở ruột gãy cảm giÃc đầy bụng nõn hay dªng để chống bệnh bÕo phš. Trong trường hợp kẹt m¶n vị kh¶ng nõn dªng. Dung dịch keo alginat cµ tÚnh dÚnh bÃm vÁ bao nõn ứng dụng để trị loÕt vÁ bảo vệ niõm mạc đường tiõu hµa. Calci alginat cµ tÚnh cầm mÃu nhanh được dªng khi chảy mÃu cam, chảy mÃu răng hoặc cÃc trường hợp chảy mÃu do bị thương tÚch. Trong kỹ nghệ dược phẩm, acid alginic vÁ alginat được dªng lÁm tà dược ră trong viõn nÕn, chất ổn định nhũ dịch cÃc kem vÁ thuốc mỡ. Trong mỹ phẩm, tÚnh chất nhũ hµa vÁ giữ nước của alginat cũng được khai thÃc. Trong c¶ng nghiệp thực phẩm một lượng lớn alginat được tiõu thụ, ngoÁi ra cÃc ngÁnh khÃc như vải sợi, sơn, giấy ... cũng cần đến alginat. (Back to top) Spirulina đă được coi lÁ một loại thức ăn mÁ nhiều nước phÃt triển đưa vÁo nu¶i trồng c¶ng nghiệp vÁ sử dụng rộng răi dưới nhiều dạng chế phẩm khÃc nhauPECTIN, NHỮNG CHẤT PECTINPectin lÁ dẫn xuất polysaccarit, phãn tử của chºng bao gồm cÃc đơn vị mắt xÚch acid α-D-galacturonic. CÃc đơn vị nÁy nối với nhau nhờ liõn kết glucosit 1-4. Mỗi đơn vị mắt xÚch chứa một nhµm cacboxyl ở vị trÚ C6. CÃc nhµm acid nÁy tồn tại ở trạng thÃi tự do hoặc dưới dạng liõn kết este (metyl este). Trong pectin tự nhiõn cµ khoảng 3/4 số nhµm acid bị metyl hµa. Những chất pectin lÁ những carbohydrat cµ phãn tử lớn mÁ phần chÚnh của phãn tử cấu tạo bởi acid polygalacturonic, do đµ được xếp vÁo nhµm "polyuronid". Những chất pectin thường gặp trong cÃc bộ phận của cãy vÁ một số tảo. Đặc biệt cªi (vỏ quả giữa) của một số cãy họ Cam (Rutaceae) như Bưởi, Cam, Chanh thš hÁm lượng rất cao, cµ thể đến 30%. Người ta chia lÁm 2 loại: Những chất pectin h·a tan, cµ trong dịch tế bÁo. Protopectin lÁ dạng kh¶ng h·a tan nằm trong thÁnh tế bÁo vÁ cÃc lớp gian bÁo, đµng vai tr· chất "cốt" vÁ "xi măng". (Back to top) NHỮNG CHẤT PECTIN H̉ØA TAN. Acid pectic. Về mặt cấu tạo hµa học, phãn tử acid pectic lÁ một mạch dÁi gồm khoảng 100 đơn vị acid D-galacturonic nối với nhau theo dãy nối α-(1-4). Về mặt cấu trºc lập thể thš acid α-D-galacturonic ở dạng ghế C1. Acid pectic lÁ cơ sở của cÃc chất pectic khÃc. Acid pectic ở trong cãy cµ thể tồn tại dưới dạng muối pectat. Pectin c·n được gọi lÁ acid pectinic. Phãn tử của pectin gồm vÁi trăm đơn vị acid a-D-galacturonic nối với nhau theo dãy nối a-(1- 4) nhưng một phần hoặc toÁn bộ cÃc nhµm carboxyl đă được methyl ester hµa. Tªy theo mức độ ester hµa mÁ người ta chia ra: loại "pectin cµ nhiều nhµm methoxyl" vÁ loại "pectin cµ Út nhµm methoxyl". Loại sau cµ dưới 40% số nhµm carboxyl bị ester hµa. CÃc cãy khÃc nhau chứa pectin khÃc nhau về khối lượng phãn tử về sự phãn bố của cÃc nhµm ester vÁ mức độ ester hµa. Tuy cấu trºc của pectin đă được xÃc định như trõn nhưng một số tÁi liệu c·n cho rằng trong thÁnh phần c·n cµ thể cµ mặt cÃc ose kh¶ng phải uronic, cÃc nhµm acetyl vÁ phosphat. TÚnh chất của pectin. Pectin ở dạng bột v¶ định hšnh mÁu xÃm trắng, tan trong nước, trong formamid, trong glycerin nµng. Độ h·a tan tăng khi mức độ methyl ester hµa tăng, nếu phãn tử cÁng lớn thš độ tan giảm. Pectin kh¶ng tan trong ethanol, isopropanol, aceton nõn cµ thể dªng cÃc dung m¶i nÁy để kết tủa. Pectin bị kết tủa bởi cÃc muối đa hoà trị như đồng sunfat, ch́ nitrat hoặc acetat, sắt chlorid. Trong sản xuất người ta dªng muối nh¶m để kết tủa pectin ở pH 4, tủa mÁu vÁng lục thu được lÁ 1 cộng kết tủa giữa pectin tÚch điện ãm vÁ nh¶m tÚch điện dương. Pectin kết tủa bằng muối kim loại cµ thể tinh chế bằng cÃch rửa tủa với ethanol hoặc aceton đă acid hµa. Cµ thể điều chế pectin từ cªi (vỏ quă giữa) của bưởi như sau: cªi bưởi phơi kh¶, tÃn bột 50g, thõm 20 ml HCl 0,03N vÁ đun 1 giờ trõn nồi cÃch thủy. Dịch nµng lọc qua b¶ng, cµ thể đun lần 2 với một Út nước nµng. Khi nguội, kiềm hµa nhẹ bằng ammoniac rồi bốc hơi cÃch thủy, nếu cµ điều kiện thš bốc hơi chãn kh¶ng c·n 60ml. Thõm vÁo dung dịch sÃnh sau khi cất 2 lần thể tÚch cồn, pectin kết tủa được ly tãm. Nếu muốn cµ pectin tinh chế thš h·a tan nµng trong một lượng Út nước rồi lại tủa bằng cồn. Tủa xốp được sấy kh¶ bằng cÃch tải mỏng trõn kÚnh nhiệt độ kh¶ng quà 450C. Dung dịch pectin 0,2-1,5% khi cµ mặt 65-70% saccharose vÁ pH 3,1-3,5 thš tạo thÁnh chất đ¶ng. Định tÚnh. Định tÚnh pectin dựa vÁo phản ứng tạo thÁnh pectin hydroxamic acid rồi cho tÃc dụng tiếp với sắt ba chlorid sẽ tạo thÁnh phức kết tủa mÁu đỏ. Thuốc thử : hydroxylamin, 1,4g trong 10ml ethanol 60%; natri hydroxyd 1,4g trong 10ml ethanol 60%; acid hydrochloric 1 thể tÚch + 2 thể tÚch ethanol 95%; 2,5g sắt ba trong 10ml HCl 0,1N pha trong ethanol 60%. CÃch tiến hÁnh: h·a một Út chất thử vÁo 1ml nước, thõm 1ml thuốc thử hydroxylamin, 1ml natri hydroxyd rồi để yõn 2 phºt, thõm 1 ml dung dịch HCl vÁ 1ml thuốc thử sắt ba. Định tÚnh trõn vi phẫu: lÁm mất nước vÁ mất hoạt tÚnh cÃc enzym bằng cÃch ngãm vi phẫu trong aceton. Rửa aceton 3, 4 lần với methanol. Cho vi phẫu vÁo một hỗn hợp gồm 1ml thuốc thử hydroxylamin vÁ 1ml natrihydroxyd, quấy 5 phºt. Thõm 1ml HCl-ethanol vÁ quấy 5 phºt. Chuyển vi phẫu vÁo 2ml thuốc thử sắt ba, sau 10 phºt vớt ra vÁ quan sÃt với kÚnh hiển vi. Định tÚnh pectin dựa vÁo sự cµ mặt của acid galacturonic: lấy một Út pectin h·a tan vÁo 3-4ml nước, thõm vÁi giọt ch́ acetat kiềm 10% vÁ đun trõn nồi cÃch thủy. Đầu tiõn tạo thÁnh tủa trắng rồi dần dần cµ mÁu cam hơi đỏ. Định tÚnh dựa vÁo sự tạo thÁnh chất đ¶ng: lấy 5g pectin, thõm 50ml nước, để yõn cho pectin trương ra, thõm 25 g đường mÚa đă tÃn thÁnh bột vÁ đun s¶i 10-15 phºt. Thõm 1ml dung dịch acid citric 40%. Sau 2-3 giờ sẽ tạo thÁnh chất đ¶ng. Định lượng XÃc định hÁm lượng anhydrouronic acid bằng phương phÃp so mÁu: mẫu kiểm nghiệm sau khi loại đường (chiết bằng ethanol) được tÃc dụng với dung dịch 0,5% EDTA để loại cÃc cation hµa trị 2. Tiếp theo dªng NaOH 1N để xÁ ph·ng hµa cÃc nhµm ester (20O, 30 phºt), acid hµa đến pH 5,0-5,5 bằng acid acetic. Cho enzym depolymer hµa tÃc dụng trong 1 giờ, lọc. Cho dịch lọc tÃc dụng với acid sulfuric đậm đặc rồi với dung dịch 0,15%carbazol trong cồn. Đo mÁu ở bước sµng 520nm. Đối chiếu với đường cong mẫu của anhydrouronic acid đi từ acid galacturonic (40g acid galacturonic ~ 33,2mg anhydrouronic acid). NgoÁi ra c·n cµ thể định lượng pectin bằng phương phÃp cãn (sau khi tủa pectin bằng cÃc dung mội hữu cơ), phương phÃp đo độ quay cực, phương phÃp đo độ nhớt. TÃc động của cÃc enzym lõn pectin. CÃc enzym tÃc động lõn pectin cµ thể chia lÁm 2 loại: Pectinesterase (P.E.). Enzym nÁy cắt nhµm ester methylic để tạo thÁnh acid pectic. Enzym cắt nhỏ phãn tử (enzym depolymer hµa). loại nÁy cµ thể chia ra: Polymethyl galacturonase (P.M.G.), enzym nÁy cắt phãn tử thÁnh từng đơn vị galacturonic. Người ta c·n chia ra endopolygalacturonase lÁ enzym cắt một cÃch ngẫu nhiõn vÁo cÃc dãy nối glycosid vÁ exopolygalacturonase lÁ enzym cắt bắt đầu từ đầu mạch. Pectinlyase (P.L.) lÁ enzym cắt dãy nối (1→4) vÁ đồng thời tạo thÁnh cÃc sản phẩm chưa no. TÃc dụng của cÃc enzym lõn pectin Người ta t́m thấy cÃc enzym nÁy trong một số nấm mốc như Aspergillus niger, A.oryzae vÁ lợi dụng để loại pectin trong việc lÁm trong nước hoa quả, trong việc chế biến sợi thảo mộc. (Back to top) PECTIN KHåNG HØA TAN. Loại nÁy c·n được gọi lÁ protopectin. Nhờ cµ protopectin mÁ cÃc quả xanh cµ độ cứng nhất định. Người ta cho rằng khi quả chÚn, dưới tÃc động của protopectinase thš protopectin chuyển thÁnh pectin h·a tan nõn quả chÚn thš mềm ra, tuy nhiõn chưa cµ chứng minh đầy đủ về sự tồn tại của một enzym đặc trưng như vậy. Về mặt cấu trºc hµa học, protopectin tạo thÁnh lÁ do liõn kết những phãn tử pectin với nhau qua cầu calci, phosphat vÁ ngoÁi ra cµ cµ sự kết hợp với cellulose, với ose vÁ một số thÁnh phần khÃc của vÃch tế bÁo. CåNG DỤNG Pectin dªng lÁm thuốc cầm mÃu đường ruột, uống dung dịch 1-2%, 40-80ml trong 24 giờ. Pectin c·n dªng lÁm tÃc nhãn nhũ hµa tốt khi kết hợp với g¶m arabic. Dung dịch pectin ổn định ở m¶i trường acid nhưng kh¶ng ổn định được ở m¶i trường kiềm. Khi dªng pectin nõn lÁm ẩm với nước vÁ nõn trộn với đường hoặc glycerin để h·a tan được dễ dÁng, trÃnh vµn cục. (Back to top) POLYSACCARIT NGUỒN GỐC ĐỘNG VẬT CHITINChitin lÁ thÁnh phần chủ yếu của m¶, biểu b́ ở c¶n trªng vÁ giÃp xÃc (vỏ t¶m). Cấu tạo vÁ chức năng của chitin tương tự với cellulose. Chitin lÁ một polisaccarit mạch thẳng trọng lượng phãn tử cao cµ thể xem như lÁ dẫn xuất của xellulose, trong đµ nhµm (-OH) ở nguyõn tử C (2) được thay thế bằng nhµm axetyl amino (-NHCOCH3), cÃc đơn vị N-acetyl- D-glucosamin (N-axetyl-2-amino-2-deoxy-D-glucopyranose) được nối với nhau bởi liõn kết β-(1→4), cÃc mắt xÚch của chitin cũng được đÃnh số như của glucose.
Chitosan lÁ dẫn xuất đề axetyl hoà của chitin, Chitosan được cấu tạo từ cÃc
mắt xÚch D-glucozamin liõn kết với nhau bởi cÃc liõn kết (1→4)-glicozit, Chitosan liõn quan chặt chẽ với chitin, nung nµng chitin trong dung dịch xºt đậm đặc cÃc gốc acetyl bị khử hết vÁ chitin chuyển thÁnh chitosan. Đãy lÁ một polysaccharide mạch thẳng, polymer của cÃc phãn tử D1,4 glucosamine.Trong thiõn nhiõn, chitin c·n hiện diện dưới nhiều hšnh thức: khà tinh khiết (sãu bướm), trong cÃc lớp rất mỏng (cÃnh bướm, với hiệu ứng mÁu tuyệt vời), cªng với cÃc protein tạo thÁnh sclerotin (chất chÚnh trong bộ xương ngoÁi của c¶n trªng) .. Chitosan trong y học + Chitosan cµ khả năng thºc đẩy quà tršnh đ¶ng mÃu. CÃc muối chitosan cµ được từ pha trộn chitosan với axit hữu cơ như axit succinic hoặc lactic sẽ tÃc dụng với mÁng tế bÁo hồng cầu, tiểu cầu khiến sự hšnh thÁnh cục mÃu đ¶ng được nhanh chµng hơn. + Chitosan gần như kh¶ng gãy dị ứng vÁ cµ tÚnh chất khÃng khuẩn tự nhiõn. Nhũ tương của chitosans cµ tÃc dụng chống nấm candida albicans vÁ aspergillus nige, k» sinh trªng Leishmania infantum. Do đµ, chitosan được dªng ngoÁi da để ph·ng nhiễm trªng với vi khuẩn vÁ nấm. + Chitosan cũng cµ tÃc dụng giảm đau do khả năng ngăn chặn xung động ở cÃc mºt tận cªng cÃc dãy thần kinh cảm giÃc. + Chitosan cµ tÚnh nhầy dÚnh (mucoadhesive) nõn được sử dụng để đưa thuốc vÁo cơ thể qua da, như sử dụng với miếng dÃn insulin. + Chitosan cũng cµ thể được kết hợp với cÃc vật liệu khÃc thÁnh những composite dªng trong y khoa, vÚ dụ như loại composite giữa chitosan với hydroxyapatit được cÃc phẫu thuật viõn sử dụng để lÁm chất lÁm đầy xương sau mổ (post-operation bone filler), để sau composite nÁy phãn hủy dần khi m¶ xương mới được tạo ra. + Chitosan lÁ một tà dược quan trọng dªng để độn, dẫn thuốc, mÁng bao phim, viõn nang mềm, nang cứng, lÁm chất mang thuốc giºp thuốc tÃc dụng chậm kÕo dÁi.. + Chitosan lÁ nguyõn liệu để lÁm vật liệu y sinh như da nhãn tạo, mÁng sinh học, chất nền cho da nhãn tạo, chỉ khãu phẫu thuật, m¶ cấy ghÕp, kem chống kh¶ da, kem lột mặt để tăng độ bÃm dÚnh, kem chống tia cực tÚm * Trong chế biến thực phẩm + Chitosan lÁ một phụ gia thực phẩm tạo độ cứng, tạo keo, phãn lớp vÁ khử axit của trÃi cãy, bÃnh kẹo, nước giải khÃt, thức ăn . + MÁng bao, giấy gµi thực phẩm chitosan giºp bảo quản thực phẩm, hoa quả, rau tươi, nước giải khÃt . Ở Việt Nam, khãu bảo quản n¶ng sản, đặc biệt trÃi cãy, c·n chưa phª hợp, nõn tšnh trạng được mªa rớt già xảy ra thường xuyõn. Khoa C¶ng Nghệ Hµa Học, ĐH C¶ng Nghiệp Thực Phẩm TP Hồ ChÚ Minh, đÐ triển khai đề tÁi Chế phẩm chitosan sinh học với sản phẩm đầu tiõn lÁ MÁng bảo quản n¶ng sản bio chitosan dạng dung dịch đang được hưởng ứng. * Chitosan trong n¶ng nghiệp + Vš cµ tÚnh khÃng khuẩn, chống nấm, chitosan dªng để bảo vệ thực vật để: giºp xử l» hạt giống vÁ lÁ thuốc trừ sãu sinh học, giºp n¶ng dãn trồng cãy chống lại cÃc bệnh nấm, thuốc chống bệnh đạo ¶n, kh¶ vằn cho lºa . Theo tÚnh toÃn của ĐH Thủy sản, Nha Trang, thš với khoảng 400 ngÁn tấn t¶m xuất khẩu hằng năm, lượng phế liệu, đầu, rãu, vỏ t¶m, sẽ khoảng 70.000 tấn, lÁ nguyõn liệu để tạo ra hơn 5000 tấn chitosan cho cÃc ngÁnh sản xuất khÃc trong nước vÁ xuất khẩu. Như vậy, việc sử dụng vỏ t¶m để sản xuất chitosan giải quyết vừa lÁm ra sản phẩm Úch lợi mới cªng lºc xử l» rÃc thải thủy sản vốn gãy ¶ nhiễm m¶i trường. Người ta cho rằng Chitosan lÁ cÃc polymer glucosamine cµ ảnh hưởng đến chuyển hµa vÁ sinh học phãn tử của tế bÁo thực vật. CÃc mục tiõu di động lÁ mÁng tế bÁo vÁ nhiễm sắc thể trong nhãn. Chitosan sẽ tÃc động lõn mÁng tế bÁo, nhiễm sắc thể, DNA, cÃc kinase, cÃc phản ứng oxy hµa Do đµ, chitosan c·n dªng lÁm chất kÚch thÚch sinh trưởng, tăng năng suất cãy trồng, Trong sản xuất rượu vang, chitosan được sử dụng để tinh lọc, ngăn ngừa hư hỏng sản phẩm. + Từ 1986, Cơ quan Bảo vệ M¶i trường Hoa Kỳ (Environmental Protection Agency) đÐ cho phÕp dªng chitosan rộng rÐi tronng n¶ng nghiệp. Trong c¶ng nghiệp dệt, chitosan được dªng để: Hồ vải, cố định hšnh in hoa, ưu điểm cµ thể thay thế được hồ tinh bột bằng chitosan lÁm cho vải, sợi bền chịu được cọ xÃt, bề mặt đẹp, bền trong kiềm; Sản xuất vải chịu nước, kh¶ng bắt lửa để sản xuất đồ bảo hộ lao động; Sản xuất sợi dõt chitin-cellulose cµ khả năng bắt mÁu thuốc nhuộm rất cao . + Trong c¶ng nghiệp giấy Chitosan cµ tÃc dụng lÁm tăng độ bền của giấy, chỉ cần thõm trọng lượng bằng 1% trọng lượng của giấy thš sẽ lÁm tăng gấp đ¶i độ bền của giấy khi ẩm ướt, tăng độ nÕt khi in. CÃc loại giấy nÁy dªng lÁm giấy vệ sinh, giấy in, tºi giấy. + Trong sản xuất mỹ phẩm: Chitosan được sử dụng trong sản xuất kem chống kh¶ da, do bản chất chitosan cố định dễ dÁng trõn biểu bš da bởi những nhµm NH4+ thường được cÃc nhÁ khoa học gắn với những chất giữ nước hoặc những chất lọc tia cực tÚm. Vš vậy chitosan lÁ gạch nối giữa hoạt chất của kem vÁ da. + Trong c¶ng nghệ in, chitosan lÁ mực in sinh học (bioprinting), cÃc sản vật in sinh học nÁy khi bỏ đi sẽ tự phãn hủy sinh học kh¶ng độc hại m¶i trường. + Sử dụng chitosan để chế tạo sơn polyurethane tự phục hồi. CÃc vật liệu chitosan mÁu cµ thể được tÃi sử dụng với tªy chọn để tÃi sử dụng hoặc loại bỏ thuốc nhuộm tại mỗi bước tÃi chế, cho phÕp tÃi sử dụng polymer một cÃch độc lập với chất mÁu. + Sản xuất chất dẻo sinh học (bioplastic) cµ khả năng phãn hủy sinh học.Theo tÚnh toÃn của GiÃo sư Nicola Everett, Đại học Nottingham, thš với 1 k» l¶ vỏ t¶m, con người cµ thể tạo ra được 15 tºi mua hÁng sinh học tiện nghi vÁ thãn thiện m¶i trường. + Chitosan lÁ một chất xơ, con người kh¶ng tiõu hµa, hấp thu được nõn cµ thể thõm vÁo thực phẩm để hạn chế hấp thụ chất bÕo, tạo độ nhớt l·ng ống tiõu hµa, giºp nhu động ruột được ổn định hơn cho những người ăn kiõng, bÕo phš, đÃi thÃo đường. * Nguyễn Văn Kh¶i. Polysacarit vÁ ứng dụng cÃc dẫn xuất tan của chºng trong thực phẩm. NXB Khoa học vÁ kỹ thuật (2006) Nguyễn Văn Kh¶i. Polyme ưa nước hoà học vÁ ứng dụng. NXB Khoa học tự nhiõn vÁ c¶ng nghệ (2007). Hồ Sĩ TrÃng. Cơ sở hoà học gỗ vÁ xenluloza Tập 1, Tập 2. NXB Khoa học vÁ kỹ thuật (2003, 2004) BÁi giảng Dược liệu Tập I - 1998 Đỗ Tất Lợi - Những cãy thuốc vÁ vị thuốc Việt Nam 2003 Д.А. Муравьева - Фармакогнозия - Москва - Медицина 1991
------------------------------------------------------- Mọi th¶ng tin liõn quan đến trang web Xin vui l·ng liõn hệ theo số điện thoại 01234195602 hoặc theo địa chỉ Email: thannv@hup.edu.vn Revised: September 02, 2020 . |